Sciencefiles-Bericht zur Drosten-PCR
Die unheilige Allianz der Verschwörungstheoretiker
von Prof. Andreas Beyer, Westfälische Hochschule Gelsenkirchen, Bocholt, Recklinghausen. Beyer ist neben Prof. Ulrich Kutschera Autor der Seite AG Evolutionsbiologie im VBIO (Verband Biologie.. e.V.)
Ende Januar 2020 publizierte ein Team von Wissenschaftlern um den Virologen Christian Drosten von der Berliner Charité ein wissenschaftliches Paper, in dem es einen PCR-Test auf das neue SARS-CoV-2-Virus beschrieb (hier als Corman-Drosten-Paper bezeichnet, Corman et al. 2020). Dieser Test wird mittlerweile weltweit angewendet und wurde vielfach weiterentwickelt. Selbstverständlich kamen auch neue Tests hinzu (Stichwort „Schnelltest“ u. a.). Nun hat sich eine Gruppe von 22 Autoren um den Kreationisten Peter Borger von der Wort-und-Wissen-Vereinigung zusammengetan, um im Rahmen eines „Gutachtens“ (Peer Review) zehn „schwere Fehler“ aufzuzeigen. Dieser Text wurde am 27.11.2020 online gestellt; wir bezeichnen ihn im Folgenden als den Borger-Text . Die Autoren des Borger-Textes fahren schwere Geschütze auf: 20 Mal bezichtigen sie Corman-Drosten schwerer Fehler, sprechen zehn Mal von Mängeln („flaws“, „blemishes“, “ inadequacies“), dabei auch von krass-eklatanten Fehlern („blatant errors“) und Unzulänglichkeiten im wissenschaftlichen Design des Tests („severe / scientific design errors“). Das ist schweres Geschütz! Angesichts der Tatsache, dass solche Wortwahl in der wissenschaftlichen Literatur üblicherweise nicht vorkommt, lohnt ein Blick auf die Argumente und Autoren.
Zunächst fällt auf, dass im Autoren-Team des Borger-Textes praktisch ausschließlich fachfremde Personen vertreten sind, vom Allgemeinmediziner über den Radiologen bis hin zum 3D-Künstler! Nicht ein einziger Autor ist, wie wir noch sehen werden, firm auf dem Gebiet der diagnostischen qPCR. Unter den 22 Autoren findet sich nur ein einziger Virologe, der emeritierte Prof. Dr. Ohashi, der jedoch niemals an Corona forschte.
Zweitens führten die Autoren des Borger-Textes nicht einen einzigen Laborversuch durch. Sie argumentieren einzig „auf theoretischer Ebene“. Dies erstaunt, denn das Corman-Drosten-Paper wurde mittlerweile über 2000 Mal (wissenschaftlich!) zitiert. Der darin beschriebene Test wird weltweit vielfach angewendet und weiterentwickelt – unter anderem von einer meiner Absolventinnen (WEIL et al. 2021). Sollten der Fachwelt die behaupteten zehn „schweren Fehler“ etwa entgangen sein, während sie allein ein Team aus 22 Autoren ohne zureichende Expertise sowie ohne experimentelle Überprüfung aufdecken konnte?
Drittens ist festzuhalten, dass der Borger-Text nicht wissenschaftlich publiziert, sondern im Internet verbreitet wird. Nach Angaben des Borger-Teams sei er auch bei Eurosurveillance eingereicht worden. Aufgrund der schweren inhaltlichen Mängel ist dort jedoch nicht mit einer Publikation zu rechnen, genauso wenig wie in jedem anderen wissenschaftlichen Journal. Auch ist nicht damit zu rechnen, dass aufgrund des Borger-Textes das Corman-Drosten-Paper zurückgezogen wird, wie Borger und Koautoren dies verlangen. (Weiteres dazu unten im Text.) Im Borger-Text werden die Kritikpunkte abschießend nochmals aufgezählt, und im Folgenden wollen wir zu den Einwänden Stellung beziehen. Alle Argumente sind ausführlich  in der detaillierten Analyse nachzulesen.
in der detaillierten Analyse nachzulesen.
1. Gemäß Borger et al. seien die verwendete Primer-Konzentrationen zu hoch, und dies ohne jeden Grund. Die zu hohen Konzentrationen würden zu unspezifischen Primerbindungen und somit PCR-Amplifikaten führen. Dies würde den Test invalidieren.
Hintergrund: In einer PCR werden gezielt bestimmte DNA- (oder in einer Modifikation des Verfahrens auch RNA-) Abschnitte vervielfältigt. Bei einer diagnostischen PCR, wie hier zum Nachweis einer Corona-Infektion, ist die erfolgreiche Vervielfältigung gleichzeitig der Nachweis für das Vorhandensein des Virus. Als wichtige Bestandteile der PCR dienen sogenannte PCR-Primer. Das sind kurze synthetische, einzelsträngige DNA-Stückchen, die auf den zu vervielfältigenden Abschnitt „zielen“, da sie genau dazu passen. Bei einer qPCR kann die Vervielfältigung des Zielfragments durch Freisetzung von Farbstoff aus einer Sonde in Echtzeit verfolgt und gemessen werden (Abb. 1). PCR-Primer und Sonden sind DNA-Stückchen, die zur Ziel-DNA an bestimmten Stellen exakt passen müssen (Abb. 1). Sie werden üblicherweise in Konzentrationen von einigen 100 nM (nanomolar) eingesetzt. Im Corman-Drosten-Paper werden aber teils höhere Konzentrationen empfohlen. Borger et al. behaupten nun, dies mache den Test unspezifisch und somit unbrauchbar.
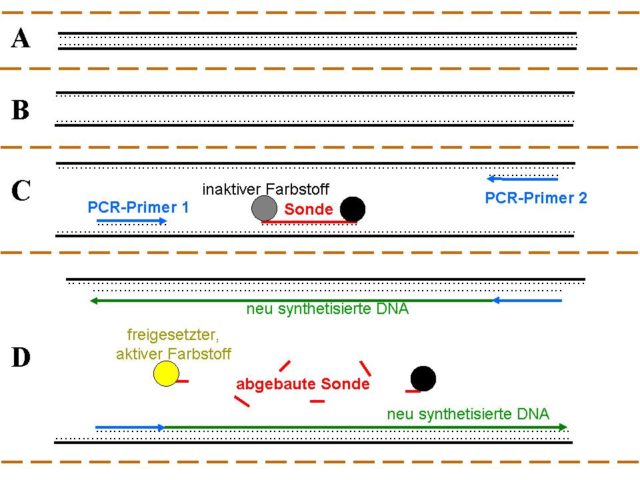
Abb. 1 Eine TaqMan-qPCR
A: Ausgangs-DNA (doppelsträngig).
B: Durch Hitze wird der DNA-Doppelstrang aufgetrennt. Die DNA liegt nun einzelsträngig vor, so dass …
C: … PCR-Primer (blau) und Sonde (rot) daran binden können. An die Sonde sind zwei Moleküle gekoppelt: Eines ist ein Farbstoffmolekül (grau), das andere ist ein Inaktivator (schwarz), der die Farbe des Farbstoffmoleküls auslöscht und ihn dadurch „maskiert“.
D: Nun findet, ausgehend von den PCR-Primern, DNA-Synthese statt, und zwar durch ein Enzym namens Taq-Polymerase (im Bild nicht gezeigt). Dadurch wird die Sonde abgebaut, wodurch der Farbstoff freigesetzt wird, was ihn aktiviert. Nun kann er – während der laufenden PCR! – gemessen werden.
Die Schritte A bis D bilden einen PCR-Zyklus; in einer qPCR werden diese Zyklenschritte bis zu 35mal wiederholt. Dabei verdoppelt sich in jedem Zyklus die Menge des PCR-Fragments. Somit verdoppelt sich auch die Menge an freigesetztem Farbstoff. Damit diese qPCR zuverlässig funktioniert, bedarf es ganz bestimmter PCR-Primer und Sonden in ganz bestimmten Konzentrationen.
Antwort: Jeder, der schon mal einen PCR-Test (insbesondere einen qPCR-Test wie im Corman-Drosten-Paper) entwarf, weiß: Die Standard-Konzentrationen sind Richtwerte, mit denen man die Etablierung des Tests beginnt. Eine Vorausberechnung der optimalen Konzentrationen ist nicht möglich: Im Rahmen der PCR-Optimierung muss man verschiedene Konzentrationen austesten. Daher liegen die finalen Konzentrationen nur selten beim Standard-Wert. Mit anderen Worten: Es ist schon im Ansatz verquer, einen Wert, der empirisch bestimmt werden muss, theoretisch (das heißt ohne Gegentests) zu kritisieren.
2. In den Sequenzen (der Primer und Sonden) existierten sechs nicht-spezifizierte („Wobbel-„) Positionen. Dadurch käme eine enorme Variabilität für die realen Labortests zustande. Ferner sei dies für die Anwender verwirrend, weswegen sich die PCR aus dem Corman-Drosten-Paper nicht für eine Standard-Diagnostik zur Identifikation des SARS-CoV-2-Virus eigne.
Hintergrund: Die PCR-Primer und Sonden (siehe Punkt 1) müssen spezifisch für ihre Zielregion, also für das zu vervielfältigende Fragment sein. Die Sequenz, also die Basenabfolge von PCR-Primern und Sonden, muss möglichst perfekt zur geplanten Bindestelle passen, sonst wird der Test unspezifisch oder unempfindlich. Nun pflegen Viren jedoch zu mutieren: Ihr Genom verändert sich. Vor allem aus diesem Grund entstehen immer wieder neue Stämme. Daher gibt es jedes Jahr neue Influenza-Epidemien.
Bevor man also eine diagnostische PCR plant, muss man alle verfügbaren Virussequenzen aus der Datenbank berücksichtigen und die PCR-Primer und Sonden an Stellen platzieren, an denen (bislang) keine Variationen aufgetreten sind. Borger et al. stellen nun fest, dass dies im Corman-Drosten-Test nicht der Fall sei: Hier gibt es in PCR-Primern und Sonden Sequenzvariationen (sog. „Wobble-Positionen“, an denen zwei verschiedene DNA-Basen auftreten können). Borger et al. behaupten, dies führe dazu, dass eine Vielzahl an Primer-Sonden-Kombinationen (mit jeweils den betreffenden Varianten) entstünde und der Test dadurch unbrauchbar würde.
Antwort: In dieser Behauptung liegen vier schwere Irrtümer von Borger und Koautoren:
I: Virale Genome mutieren nun einmal, und die sich ansammelnden Mutationen sind ungleich über das Virus-Genom verteilt: Es gibt Bereiche, die funktional besonders wichtig sind. Daher werden von der Selektion hier nur wenige Mutationen „geduldet“; diese Bereiche sind „evolutionär konserviert“. Als Zielposition für die Bindung der PCR-Primer (vgl. Punkt 1) sucht man sich diejenigen Bereiche aus, die einerseits typisch für die nachzuweisende Virengruppe sind, andererseits in eben jener Gruppe konserviert. Diesen Wunsch erfüllt einem die Natur aber leider äußerst selten, wie jeder weiß, der Erfahrung mit Virus-Diagnostik über PCR-Tests hat. Ergo muss man nehmen, was die Natur einem bietet, und das sind in aller Regel Sequenzabschnitte mit solchen „Wobbel-Positionen“. Das ist kein Design-Fehler, sondern eine schlichte Anpassung an die natürlichen Gegebenheiten.
II: Durch diese „Wobbel-Positionen“ kommen mitnichten „enorme Variabilitäten im Test“ zustande. Borger und Koautoren wissen offenbar nicht, dass die betreffenden Oligonukleotide bereits als Gemisch synthetisiert, geliefert und im Test eingesetzt werden.
III: Auch die Behauptung, solche „Wobbel-Positionen“ wären verwirrend für den Anwender, zeigt, dass Borger und Koautoren keinerlei Erfahrung mit qPCR-Systemen haben: So, wie jeder Kfz-Mechaniker weiß, was ein gekröpfter Ringschlüssel ist, kann jeder halbwegs routinierte PCR-Anwender „Wobbel-Positionen“ lesen und verstehen.
IV: Die Annahme, eine PCR mit „Wobbel-Positionen“ würde automatisch unspezifisch, ist falsch. Diese nicht spezifizierten „Wobbel-Positionen“ müssen bei der Etablierung und Validierung des Tests berücksichtigt werden. Für HIV-Tests ist dieses Vorgehen seit Jahrzehnten Standard. Aus diesen Gründen gehören Oligonukleotide mit „Wobbel-Positionen“ zu Standard-Repertoire der PCR-Diagnostik auf Viren, was Borger und Koautoren offenbar nicht wissen.
3. Der Corman-Drosten-Test könne nicht zwischen kompletten und fragmentierten Virusgenomen unterscheiden. Er sei untauglich zur Detektion infektiöser Viren, was ihn als Test auf SARS-CoV-2 entwerte.
Hintergrund: Pathobiologisch aktiv (und somit ansteckend) sind nur Viren mit intaktem Genom. Der Corman-Drosten-Test weist aber nur das Vorhandensein von zwei bestimmten, kurzen Abschnitten des SARS-CoV-19 Genoms nach. Also weist der Test auch fragmentierte und somit inaktive, ungefährliche Genomkopien nach.
Antwort: Dieses Argument ist verfehlt. Zum einen kann kein einziger Test komplette von fragmentierten Virusgenomen unterscheiden. Andererseits ist dies auch nicht nötig: Jedes virale Genom – ob komplett oder fragmentiert, ob intakt oder defekt, ob ursprüngliche Version oder mutiert – entstammt einer infizierten Zelle. Wie der Infektiologe und Virologe weiß, wird jede im Patienten nachgewiesene virale Genomkopie Indikator einer Infektion sein, sobald eine bestimmte Schwelle (also Anzahl nachgewiesener Genomkopien) überschritten ist.
Im Übrigen könnte man mit dem gleichen „Argument“ auch auf Freispruch eines Täters plädieren, wenn am Tatort „nur“ dessen Fingerabdrücke, Blutspuren und Kleidungsstücke, nicht aber die Tat als solche beobachtet wurde. Das ist absurd.
4. Die Autoren behaupten, die PCR-Primer RdRp_SARSr_F und RdRp_SARSr_R hätten um 10°C voneinander abweichende Annealing-Temperaturen. Der PCR-Test zum Nachweis von SARS-CoV-2 sei deshalb untauglich.
Hintergrund: Ein besonders wichtiger Schritt bei der PCR ist das Anbinden, das Andocken (Fachbegriff „Annealing“) der PCR-Primer (vergl. Punkt 1) an ihre Zielabschnitte (hier: im Virusgenom). Dieser Prozessschritt ist temperaturabhängig: Bei zu hoher Temperatur (das heißt, wenn die Annealing-Temperatur zu hoch gewählt wird), können die PCR-Primer nicht binden. Ist sie zu niedrig, binden die PCR-Primer auch unspezifisch, also an Stellen, an denen sie nicht binden sollen. Um hier höchstmögliche Spezifität zu gewährleisten, wird man die beiden PCR-Primer physikochemisch möglichst ähnlich gestalten. Allerdings sei bei einem der Primersysteme, so der Borger-Text, die Differenz zwischen beiden PCR-Primern viel zu hoch.
Antwort: Zunächst verwechseln Borger et al. die Begriffe: Die Annealing-Temperatur ist für beide Primer gleich, das geht auch gar nicht anders! Lediglich die Schmelztemperaturen der beiden Primer unterscheiden sich. In der Tat sollten diese beiden Werte möglichst ähnlich sein. Jeder, der Erfahrung mit PCR-Systemen hat, weiß aber, dass die Gegebenheiten der vorliegenden Sequenzen das Machbare diktieren: Größere Abweichungen von den optimalen Werten sind manchmal unvermeidbar! Auch aus diesem Grunde führt kein Weg am gründlichen Austesten und Optimieren der PCR-Bedingungen vorbei, was Drosten und Koautoren auch getan haben.
5. Ein schwerwiegender Fehler sei, dass versäumt wurde, einen Ct-Wert anzugeben, der zwischen positivem und negativem Testergebnis unterscheide. Auch darum sei der Test ungeeignet, das SARS-CoV-2 Virus nachzuweisen.
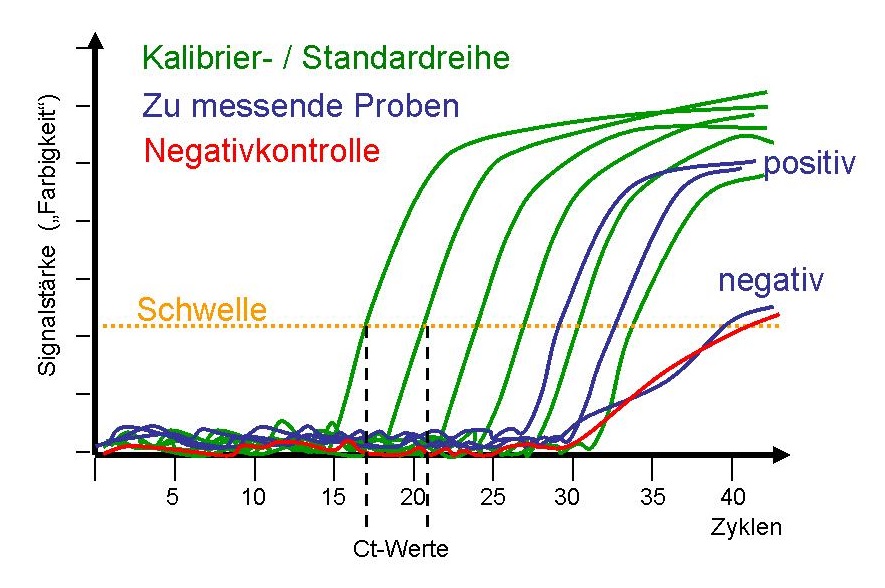
Hintergrund: Die Vermehrung betreffender Zielabschnitte des viralen Genoms über PCR (genauer Fachbegriff: TaqMan-qPCR) sorgt dafür, dass im PCR-Prozess ein Fluoreszenzfarbstoff entsteht, der während des laufenden PCR-Prozesses gemessen wird. Anfangs ist noch zu wenig davon vorhanden, so dass der Farbstoff erst später im Verlauf der PCR messbar ist. Also erst, wenn der Farbstoff eine gewisse Menge erreicht, überschreitet das gemessene Signal eine bestimmte Schwelle, und er kann detektiert werden. Den Punkt, an dem diese Überschreitung der Schwelle passiert, nennt man Ct-Wert (Abb. 2). Es sei, so Borger et al., eine grobe Unterlassung, dass im Corman-Drosten-Paper dieser Ct-Wert nicht definiert werde.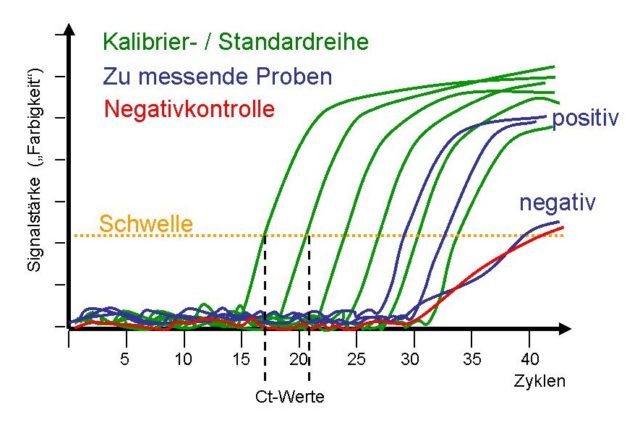
Abb.2: qPCR-Amplifikationskurve. Jede Linie entspricht einem individuellen PCR-Ansatz; gezeigt sind die Messwerte (faktisch die Farbstoffentwicklung) über die Zyklen.
grün: Eine Verdünnungsreihe mit bekannten Mengen des zu vervielfältigenden DNA-Stücks. Das ist die Kalibrier- oder Standardreihe. Sie ist gleichzeitig eine Positivkontrolle, denn diese Ansätze müssen ein positives Ergebnis bringen, und zwar mit Kurven in definierten, vorhersehbaren Abständen.
rot: Negativkontrolle, also ein Ansatz ohne DNA – oder mit solcher DNA, die nicht zu den PCR-Primern passt, also nicht vervielfältigt werden kann.
blau: Drei zu messende Ansätze, von denen zwei positiv sind und einer negativ. Bei den positiven Ansätzen ermöglicht der Vergleich mit der Kalibrierreihe die Bestimmung der in den Proben vorhandenen Ziel-DNA.
orange: Schwellenwert („Threshold“). Genau dort, wo die Kurve diese Schwelle überschreitet, wird für diesen Ansatz die Zyklenzahl abgelesen: Das ist dann der Ct-Wert (eingezeichnet für die ersten beiden grünen Kurven).
Der Verlauf der Kurven muss eine typische Gestalt haben: zuerst unregelmäßig bei kleinen Werten (das ist das Hintergrundrauschen, wenn in den ersten Zyklen noch nicht genügend Farbstoff gebildet wurde), dann ansteigend in eine lineare („gerade“) Phase, die dann Richtung Horizontale abknickt. Genau dadurch kann man echte Positivwerte auch von Negativwerten unterscheiden, bei denen die Kurve flach bleibt und nur ganz am Ende ohne den beschriebenen, charakteristischen Verlauf langsam ansteigen.
Antwort: Zunächst einmal verwechseln Borger et al. die Begriffe: Den Ct-Wert kann man gar nicht angeben, denn er wird gemessen. Gemeint ist wohl der Schwellenwert, der anzugeben sei. Aber auch das ist unsinnig, weil diese Schwelle vom Detektionssystem (unter anderem also vom Gerät) abhängt. Borger et al. scheinen nicht zu wissen, wie man eine qPCR durchführt: Parallel zu den Proben lässt man eine Kalibrierreihe „mitlaufen“: Zusammen mit den Proben prozessiert man also eine Verdünnungsreihe, eine Serie von Proben mit bekannter Virus-Menge; erst der Vergleich mit den Ct-Werten dieser Reihe erbringt das Ergebnis.
6. Die PCR-Produkte seien auf molekularer Ebene nicht (durch gelelektrophoretische Analyse) validiert worden. Dadurch sei der Test unbrauchbar.
Hintergrund: Bei einer PCR wird ein Zielfragment aus einer DNA (hier: aus dem SARS-CoV-2 Genom) vervielfältigt (Fachbegriff „amplifiziert“). Standardvorgehen ist, dass ein PCR-Ansatz am Ende auf einem Agarosegel analysiert wird: Dort kann man die Länge der gebildeten Fragmente sichtbar machen.
Antwort: Selbstverständlich wurden die PCR-Fragmente zu Beginn der Entwicklungsarbeiten gelelektrophoretisch analysiert! Das macht man immer so, aber es bedarf hier keiner Erwähnung: Die Spezifität bei einer solchen qPCR ist wegen der drei voneinander unabhängigen Oligonukleotide recht hoch (vgl. Punkt 1). Außerdem beschreibt das Corman-Drosten-Paper die Validierung in aller Ausführlichkeit.
7. Der Corman-Drosten-Test beinhalte weder eine eindeutig benannte Positivkontrolle um die Spezifität für SARS-CoV-2 nachzuweisen, noch eine Negativkontrolle um die Anwesenheit anderer Coronaviren auszuschließen.
Hintergrund: Bei jedem analytischen Test – und erst recht bei diagnostischen Tests – lässt man sogenannte Kontrollen mitlaufen. Positivkontrollen sind standardisierte Ansätze, in denen die nachzuweisende Substanz (hier: das SARS-CoV-2 Genom) in bekannter Menge / Konzentration enthalten ist. Dieser Ansatz muss ein positives Ergebnis erbringen; somit überprüft man in jeden Testdurchlauf das Funktionieren des Tests. Negativkontrollen enthalten keinen (oder „falsche“) Analyten , also keine Kopie des SARS-CoV-2-Genoms. Dieser Ansatz darf kein positives Ergebnis erbringen. So überprüft man, ob es Kontaminationen gegeben hat, ob also sauber gearbeitet wurde.
Antwort: Das Gegenteil ist wahr, das Corman-Drosten-Paper benennt mehrere Positiv- und Negativkontrollen und beschreibt ausführlich die Validierung der Test-Spezifität. Die konkrete Auswahl und „Konfektionierung“ der Kontrollen obliegt dem Anwender bei Etablierung des qPCR-Systems, wenn er eine SOP definiert (vgl. Punkt 8). So ist das übliche Vorgehen.
8. Das Testdesign im Corman-Drosten-Paper sei vage und mangelhaft, so dass es [vom Anwender] dutzendfach unterschiedlich interpretiert werden könne. Nichts sei standardisiert, und es gäbe keine SOP (Standard Operation Procedure = Standard-Protokoll). Damit sei die wissenschaftliche Qualität hochgradig fragwürdig und der Test unbrauchbar zur Identifikation des SARS-CoV-2-Virus.
Hintergrund: Wenn – wie hier im Corma-Drosten-Paper – ein diagnostischer Test publiziert wird, müssen logischerweise alle Angaben vorhanden sein, die es dem Anwender ermöglichen, diesen Test im eigenen Labor zu etablieren und durchzuführen.
Antwort: Die Behauptungen sind zu einer Hälfte unwahr, zur anderen Hälfte gehen sie am Thema vorbei: Tatsächlich benennt das Corman-Drosten-Paper allerelevanten Parameter: Oligonukleotid-Sequenzen und -Konzentrationen, Salzbedingungen, dNTP-Konzentrationen und PCR-Zyklusbedingungen. SOPs sind hingegen auch (und in erheblichem Maße) abhängig von den örtlichen Gegebenheiten. Daher muss jeder diagnostische Test in jedem Labor erneut etabliert werden. Dazu gehört auch die Abfassung einer SOP. Auch hier zeigt sich, dass den Autoren des Borger-Testes jedwede Erfahrung mit diagnostischen Testsystemen fehlt.
9. Das Corman-Drosten-Paper erfuhr keine unabhängige Begutachtung. Auch deshalb sei die Qualität der Arbeit zweifelhaft.
Hintergrund: Wenn bei einem wissenschaftlichen Journal eine Publikation eingereicht wird, so wird sie einer unabhängigen Prüfung durch mehrere Fachleute unterzogen, und zwar anonym (die Autoren erfahren niemals die Namen der Gutachter). Dies dient der Qualitätskontrolle. Da das Manuskript einen Tag nach Einreichen akzeptiert wurde, könne es – so Borger et al. – nicht begutachtet worden sein, sei also unbesehen publiziert worden.
Antwort: In der Tat dauert ein Begutachtungsprozess mehrere Tage oder sogar Wochen. Allerdings ist das Journal Eurosurveillancefür seine Schnelligkeit bekannt. Wenn eine Publikation ansteht, bei der sich Autoren und Journal über die Dringlichkeit einig sind, wird manchmal ein beschleunigtes Verfahren durchgeführt: Entweder, es wird dafür gesorgt, dass die Gutachter an Tag und Stunde der Einreichung bereitstehen. Oder die Begutachtung der Publikation erfolgt in Teilen – es wird laufend alles begutachtet, was eingereicht wird. In diesem Fall ist das in der Publikation vermerkte Datum der Einreichung der Tag, an dem das letzte Dokument eingereicht wurde – etwa Material, das die Gutachter noch nachgefordert haben. In einem solchen Fall kann der vermerkte Tag der Einreichung gleichzeitig der Tag sein, an dem die Publikation akzeptiert wurde. Übrigens: In diesem speziellen Fall stand den Gutachtern das Corman-Drosten-Paper bereits eine Woche vor der offiziellen Einreichung über einen sogenannten Preprint-Server zur Verfügung.
10. Es gäbe Interessenskonflikte. Erstens seien Christian Drosten und Chantal Reusken Mitherausgeber (Editoren) von Eurosurveillance, wo das Corman-Drosten-Paper veröffentlicht wurde. Zweitens wären mehrere Autoren an Biofirmen beteiligt, die (durch Verkauf von Testkits und Reagenzien) wirtschaftliche Vorteile aus dem publizierten Test zögen.
Hintergrund: Es ist wissenschaftsethisch inakzeptabel, wenn man persönliche Vorteile aus einer Publikation oder Tätigkeit zieht, ohne dies offenzulegen und klar zu benennen. Man darf sich keine Vorteile verschaffen, indem man im eigenen Journal publiziert und dabei die eigene „Hausmacht“ nutzt, um z. B. den Begutachtungsprozess zu eigenen Gunsten zu beeinflussen. Es ist auch verwerflich, durch eine Publikation eigene Produkte zu bewerben oder ihnen Marktvorteile zu verschaffen.
Antwort: Es ist nicht verboten und auch nicht wissenschaftlich fragwürdig, dass Wissenschaftler in Journalen publizieren, in denen sie Editoren sind. Die Journale haben hierfür eigene Prozeduren definiert: Die betreffenden Editoren/Autoren werden konsequent vom Begutachtungs- und Publikationsprozess ausgeschlossen. Was die Anschuldigungen in Bezug auf wirtschaftliches Eigeninteresse anbelangt, so ist festzuhalten, dass der Corman-Drosten-qPCR-Test mit besagter Publikation offengelegt wurde. Die Autoren haben den Test weder mit einem Patent noch mit einem Gebrauchsmusterschutz oder ähnlichem belegt. Er ist frei verfügbar, so dass jeder die Primer und Reagenzien beziehen kann, von wem er will. Es ist schwer, hier nicht von böswilliger Verleumdung zu sprechen. Abgesehen davon fragt man sich, was diese Anschuldigungen – unabhängig davon ob sie zuträfen oder nicht – mit der Qualität und Zuverlässigkeit des Tests zu tun haben sollten.
Im Lichte der Analyse des Corman-Drosten-qPCR-Protokolls zum Nachweis von SARS-CoV-2 hätten Borger und Koautoren schwerste Mängel nachgewiesen, aufgrund derer der Test unbrauchbar sei.
Man fragt sich, warum all diese Mängel in der mittlerweile 3/4jährigen Anwendung weltweit keinem Experten aufgefallen sind. Und man fragt sich, wie es 22 weitestgehend bis vollständig fachfremden Autoren gelungen sein soll, schwerste Mängel „festzustellen“, ohne das qPCR-System euch nur ein einziges Mal im Labor getestet zu haben!
Interessanterweise verschweigen Borger et al. (oder sie haben schlicht keine Ahnung), dass systematische (experimentelle!) Vergleiche zwischen verschiedenen PCR-Systemen publiziert wurden (z. B. AFZAL 2020; MATHEEUSSEN et al. 2020; NALLA et al. 2020; VOGELS et al. 2020), in denen keinerlei schwere Mängel festgestellt wurden. Ganz im Gegenteil muss man schwerste Mängel bis hin zu ehrabschneidenden Behauptungen im Borger-Text konstatieren. Dies reicht bis zu Anfänger-Fehlern in der Analyse der Primersequenzen sowie bei der Berechnung der Konzentrationen (Details in der  ausführlichen Widerlegung).
ausführlichen Widerlegung).
Wie mangelhaft Borgers Expertise im Bereich der Molekularbiologie ist, zeigt sich auch im  W+W-Disk.-Beitr. 3/20 („Covid-19 und mRNA-Impfstoffe – eine kleine Orientierungshilfe“), wo im Abschnitt Der mRNA-Impfstoff mRNA-Impfstoffe und rekombinante Impfviren vermengt und verwechselt werden.
W+W-Disk.-Beitr. 3/20 („Covid-19 und mRNA-Impfstoffe – eine kleine Orientierungshilfe“), wo im Abschnitt Der mRNA-Impfstoff mRNA-Impfstoffe und rekombinante Impfviren vermengt und verwechselt werden.
Literatur
AFZAL, A. (2020) Molecular diagnostic technologies for COVID-19: Limitations and challenges. Journal of advanced research 26, S. 149-159. Doi: https://doi.org/10.1016/j.jare.2020.08.002.
BORGER, P.; MALHOTRA, B. R.; Yeadon, M.; CRAIG, C.; McKERNAN, K.; STEGER, K.; McSHEEHY, K.; ANGELOVA, L.; FRANCHI, F.; BINDER, T.; ULLRICH, H.; OHASHI, M.; SCOGLIO, S.; DOESBURG-van-KLEFFENS, M.; GILBERT, D.; KLEMENT, R.; SCHRUEFER, R.; PIEKSMA, B. W.; BONTE, J.; DALLE CARBONARE, B. H.; CORBETT, K. P. & KÄMMERER, U. (2020) External peer review of the RTPCR test to detect SARS-CoV-2 reveals 10 major scientific flaws at the molecular and methodological level: consequences for false positive results. https://cormandrostenreview.com/report/
CORMAN, V. M.; LANDT, O.; KAISER, M.; MOLENKAMP, R.; MEIJER, A.; CHU, D. K.; BLEICKER, T.; BRÜNINK, S.; SCHNEIDER, J.; SCHMIDT, M. L.; MULDERS, D. G.; HAAGMANS, B. L.; van der VEER, B.; van den BRINK, S.; WIJSMAN, L.; GODERSKI, G.; ROMETTE, J. L.; ELLIS, J.; ZAMBON, M.; PEIRIS, M.; GOOSSENS, H.; REUSKEN, C.; KOOPMANS, M. P. & DROSTEN, C. (2020) Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveillance 25(3), 2000045. Doi: https://doi.org/10.2807/1560-7917.ES.2020.25.3.2000045.
MATHEEUSSEN, V.; CORMAN, V. M.; DONOSO MANTKE, O.; McCULLOCH, E.; LAMMENS, C.; GOOSSENS, H.; NIEMEYER, D.; WALLACE, P. S.; KLAPPER, P.; NIESTERS, H. G.; DROSTEN, C.; LEVEN, M. & RECOVER project and collaborating networks (2020) International external quality assessment for SARS-CoV-2 molecular detection and survey on clinical laboratory preparedness during the COVID-19 pandemic, April/May 2020. Euro Surveillance 25(27), 2001223. Doi: https://doi.org/10.2807/1560-7917.ES.2020.25.27.2001223.
NALLA, A. K.; CASTO, A. M.; HUANG, M.-L. W.; PERCHETTI, G. A.; SAMPOLEO, R.; SHRESTHA, L. et al. (2020) Comparative performance of SARS-CoV-2 detection assays using seven different primer-probe sets and one assay kit. Journal of Clinical Microbiology 58(6), e00557-20. Doi: https://doi.org/10.1128/JCM.00557-20.
VOGELS, C. B. F.; BRITO, A. F.; […] & GRUBAUGH, N. D. (2020) Analytical sensitivity and efficiency comparisons of SARS-CoV-2 RT-qPCR primer-probe sets. Nature Microbiology 5(10), S. 1299-1305. Doi: https://doi.org/10.1038/s41564-020-0761-6.
WEIL, P. P. et al (2021) Combined RT-qPCR and Pyrosequencing of a SARS-CoV-2 Spike Glycoprotein Polybasic Cleavage Motif Uncovers Rare Pediatric COVID-19 Spectrum Diseases of Unusual Presentation. Doi: https://doi.org/10.1101/2020.12.19.20243428.
—
Unser Kommentar zur Kritik von Prof. Beyer (ARG):
Tatsache ist, daß Christian Drosten mit seinen Förder-Millionen schon gute Virologen und Laborwissenschaftler einkaufen kann, die die Reputation seiner Professur/Abteilung erarbeiten. Eine mittlerweile an deutschen Universitäten übliche Situation: Der Gruppenchef ist ein guter Politiker; und seine stillen Doktoren, Doktoranden und T-Assistenten machen die tägliche Laborarbeit und veröffentlichen diese.
Nichtsdestotrotz ist die halb-quantitative RT-PCR und allgemein die qualitative PCR natürlich keine Methode, um eine Infektion oder gar Erkrankung nachzuweisen; bestenfalls ein Hinweis für weitere Methodik. Der „Massenausbruch“ bei Tönnies, wo Corona-haltige Rinder und Pferde zerlegt wurden, zeigt sehr deutlich, daß PCR alle möglichen C-Viren nachweisen kann (und tut). Der Hinweis auf die mangelnde Fachkenntnis der Autoren um Pieter Borger ist unserer Ansicht nach heftig übertrieben, da mehrere Ärzte (auch eine Virologin!) und Biochemiker/ Laborchemiker unter den Autoren sind. Beispiele:
Dr. Pieter Borger (MSc, PhD), Molekulargenetik, W + W Research Associate, Lörrach, Deutschland
Dr. Michael Yeadon BSs (Hons) Biochem Tox U Surrey, PhD Pharmakologie U Surrey. Geschäftsführer, Yeadon Consulting Ltd, ehemaliger Pfizer Chief Scientist, Großbritannien
Dr. Clare Craig MA, BM (Cantab), Bachelor Chemie (Oxon), FRCPath, Vereinigtes Königreich
Kevin McKernan von der BS Emory University, wissenschaftlicher Leiter und Gründer von Medical Genomics, hat die Sequenzierungspipeline am WIBR / MIT für das Humangenomprojekt entwickelt, den SOLiD-Sequenzer erfunden und entwickelt und Patente für PCR, DNA-Isolierung und Sequenzierung in den USA erteilt
Dr. Paul McSheehy (BSc, PhD), Biochemiker und Industriepharmakologe, Loerrach, Deutschland 8) Dr. Lidiya Angelova, MSc in Biologie, PhD in Mikrobiologie, ehemaliger Forscher am Nationalen Institut für Allergie und Infektionskrankheiten (NIAID), Maryland, USA
Prof. Dr. Makoto Ohashi, emeritierter Professor, PhD in Mikrobiologie und Immunologie, Tokushima University, Japan
Dr. Marjolein Doesburg-van Kleffens (MSc, PhD), Facharzt für Labormedizin (klinische Chemie), Maasziekenhuis Pantein, Beugen, Niederlande
Dr. Ruth Schruefer, PhD, Humangenetik / Immunologie, München, Deutschland,
Dr. Bruno H. Dalle Carbonare (Molekularbiologe), IP-Spezialist, BDC Basel, Schweiz
Prof. Dr. Ulrike Kämmerer, Fachärztin für Virologie / Immunologie / Humanbiologie / Zellbiologie, Universitätsklinikum Würzburg
Update der EIKE Redaktion
Ulrike Kämmerer hat hier auf Rubikon zu ähnlicher Kritik schon einmal Stellung genommen. Mit Dank an Leserin Christine Full
Gunnar Kaiser hat ein gut verständliches Video zur Drosten-PCR publiziert, das einige der Argumente von Prof. Beyer betrifft.
















Wir freuen uns über Ihren Kommentar, bitten aber folgende Regeln zu beachten:
- Bitte geben Sie Ihren Namen an (Benutzerprofil) - Kommentare "von anonym" werden gelöscht.
- Vermeiden Sie Allgemeinplätze, Beleidigungen oder Fäkal- Sprache, es sei denn, dass sie in einem notwendigen Zitat enthalten oder für die Anmerkung wichtig sind. Vermeiden Sie Schmähreden, andauernde Wiederholungen und jede Form von Mißachtung von Gegnern. Auch lange Präsentationen von Amateur-Theorien bitten wir zu vermeiden.
- Bleiben Sie beim Thema des zu kommentierenden Beitrags. Gehen Sie in Diskussionen mit Bloggern anderer Meinung auf deren Argumente ein und weichen Sie nicht durch Eröffnen laufend neuer Themen aus. Beschränken Sie sich auf eine zumutbare Anzahl von Kommentaren pro Zeit. Versuchte Majorisierung unseres Kommentarblogs, wie z.B. durch extrem häufiges Posten, permanente Wiederholungen etc. (Forentrolle) wird von uns mit Sperren beantwortet.
- Sie können anderer Meinung sein, aber vermeiden Sie persönliche Angriffe.
- Drohungen werden ernst genommen und ggf. an die Strafverfolgungsbehörden weitergegeben.
- Spam und Werbung sind im Kommentarbereich nicht erlaubt.
Diese Richtlinien sind sehr allgemein und können nicht jede mögliche Situation abdecken. Nehmen Sie deshalb bitte nicht an, dass das EIKE Management mit Ihnen übereinstimmt oder sonst Ihre Anmerkungen gutheißt. Wir behalten uns jederzeit das Recht vor, Anmerkungen zu filtern oder zu löschen oder zu bestreiten und dies ganz allein nach unserem Gutdünken. Wenn Sie finden, dass Ihre Anmerkung unpassend gefiltert wurde, schicken Sie uns bitte eine Mail über "Über Uns->Kontakt"Was auch auffällt: Dr. Beyer, haben Sie das Addendum gar nicht bemerkt? Dort wird auf ein paar Ihrer Argumente eingegangen. Oder ist Ihr Kommentar deutlich früher entstanden?
Hallo zusammen,>> [Gunnar Kaiser-Video 1:50] Die Corona-Gefahr sei nicht vorhersehbar gewesen.Doch. Schon Dezember 2019 war klar, dass SARS-CoV-2 ein enger Verwandter von SARS-CoV-1 war, musste man mit hohe Pathogenität befürchten, daher war ein früher Test sinnvoll.<<>> [Gunnar Kaiser-Video 2:00] Die Autoren des Borger-Textes seien Fachleute, seien Forscher.<<Sie sind in Bezug sowohl auf Corona als auch auf qPCR Laien – siehe http://ag-evolutionsbiologie.net/pdf/2021/Drosten-PCR-Borger-Report.pdf>> [Gunnar Kaiser-Video 3:30ff] Das qPCR-Protokoll sei untauglich.<<Naja … einfach al meine Analyse lesen (s.o.) oder en detail unter http://evolutionsbiologie.net/pdf/2021/Drosten-PCR-Borger-Report.pdf
Dass damals eine hohe Pathogenität erwartet wurde, wurde damals von Dr. Drosten aber nicht so kommuniziert. Und meines Wissens auch von Eurosurveillance und der WHO nicht.
Und ein Verweis darauf, dass die Wissenschaftler keine Molekularbiologen sind, heißt nicht, dass sie Laien in Bezug auf qPCR sind. qPCR ist eine Standardmethode in Laboren, das lernen nicht nur Molekularbiologen.
Neulich sagte Laschet, dass die Inzidenzwerte reine Erfindungen der Politik sind. Konkret bezog sich der NRW-Ministerpräsident damit auf die Willkür-Beschlüsse von vergangener Woche.Er nannte die politisch definierten Grenzwerte „erfunden“ – was nicht weniger heißt, als dass es sich bei den Lockdown-Begründungen um einen Schwindel handelt.Er wird es ja schließlich selber wissen, weil er immer bei den Besprechungen dabei ist. Nun hat der aber die Regierung entlarvt. Eigentlich wissen das schon fast Alle.Die Reaktionen kamen selbstverständlich sofort. CDU-Chef Armin Laschet ist mit skeptischen Äußerungen zur Bedeutung von Corona-Inzidenzzahlen auf Kritik bei SPD und Grünen gestoßen. „Wer wie Laschet von ‚erfundenen Grenzwerten‘ spricht, der zerstört Vertrauen in die Corona-Maßnahmen“Wie Herr Maaßen, der sich gegen das Narrativ der Regierung stellte. Herr Maaßen hatte nämlich auch das Vertrauen in die Medien und an Frau Merkel zerstört. Das könnte auch dementsprechend für Herrn Laschet gewisse Folgen haben.
Das ist eine andere Frage, die nichts mit dem PCR-Test und allgemein dem Viren-Nachweis zu tun hat.
Grüße
Andreas Beyer
Bitte anderen Texteditor verwenden. Zuviele Steuerzeichen zu löschen.
Ein Begutachtungsprozess von max. 48 h ist lächerlich und man fragt sich, warum die Gutachter so etwas mitmachen. Selbst wenn eine noch unvollständige Version bereits eine Woche vor der Freigabe zur Verfügung stand, sind Zweifel an der wissenschaftlichen Integrität der Beteiligten (Herausgeber, Autoren, Gutachter) sehr berechtigt. Begutachtungen erfordern umfangreiche Recherchen, die erhebliche Zeit in Anspruch nehmen. Ein nicht zu vernachlässigender Zeitfaktor liegt im Nachdenken. Oder haben die Gutachter nur formal gewirkt und nicht inhaltlich geprüft?
„und nicht inhaltlich geprüft? “ Bei DEM Stallgeruch des Autors wahrscheinlich. Da traut sich keiner, zu widersprechen.
[Heino Müller] Ein Begutachtungsprozess von max. 48 h ist lächerlich.<<
Man schaue in http://evolutionsbiologie.net/pdf/2021/Drosten-PCR-Borger-Report.pdf
Fest steht, die WHO hat inzwischen erkannt und einen Tag nach Bidens Vereidigung bekannt gegeben, das der cT Wert von 45 zu hoch ist, und es anderer Kriterien bedarf um bei einem in dem Fall positiven PCR Test tatsächlich auf eine Infektion zu schließen.
>> [Krishna Gans] … die WHO hat inzwischen erkannt und einen Tag nach Bidens Vereidigung bekannt gegeben, das der cT Wert von 45 zu hoch ist.<<
Sorry, aber das ist Quatsch – so funktioniert qPCR nicht. Man legt keine Ct-Werte fest, man misst sie. Und zwar in Relation zu einer Kalibrierreihe. Einfach mal oben nachlesen oder in der Detailanalyse.
Bei Rubikon gibt es ein aktuelles Interview mit Ulrike Kämmerer zum Gutachten des PCR-Tests von drosten et al. Dort wird auch beantwortet, warum das Gutachten im Internet veröffentlicht wurde.
https://www.rubikon.news/artikel/spates-echo
Danke, haben wir im Haupttext ergänzt.
Schon die Einleitung des Artikels von Andreas Beyer sind mir negativ aufgestoßen.1. Zitat : „Nun hat sich eine Gruppe von 22 Autoren um den Kreationisten Peter Borger von der Wort-und-Wissen-Vereinigung zusammengetan…“ Mit dem Ausdruck Kreationist wollte beyer die Studie schon von Anfang an in das Feld der geistig völlig abgerdrehten Mitmenschen einordnen, denen man per se nichts glauben darf.2. Zitat: „Unter den 22 Autoren findet sich nur ein einziger Virologe, der emeritierte Prof. Dr. Ohashi, der jedoch niemals an Corona forschte.“Dazu zitiere ich mal aus der Vita von Professor Dr. Ulrike Kämmerer (Uni Würzburg): “ Prof. Dr. Ulrike Kämmerer, Biologin mit 30 Jahren Laborerfahrung in der universitären medizinischen Forschung. Diplomarbeit in Virologie, Promotion über Virusnachweise bei Herzmuskelerkrankungen mittels RT-PCR, Habilitation im Bereich Reproduktions-Immunologie, seit 10 Jahren Apl. Professorin, durchgehend in der klinischen Laborforschung …“Den Rest des Textes von beyer habe ich dann nur überflogen, denn wer schon bei einfachsten Sachverhalten solche Fehler macht …
Stimmt, das mit den Kreationisten tut hier nichts zur Sache; ist wohl aber Motiv.
Ich weiß. Verschwörungstheoretiker dürfen ihre Gegner herabwürdigen (man schaue sich einfach mal die Wortwahl im Borger-Text an), aber wenn man ihnen dann aufzeigt, wo sie falsch liegen, wo ihre eigene Expertise mangelt und welchen Background sie haben, ist das ein ad hominem Argument. Und, nein, Kämmerer ist KEINE Virologen, weil sie vor Jahrzehnten mal eine virologische Diplomarbeit geschrieben hat. Ich habe 1997 als alleiniger Autor ein bioinformatisches Paper publiziert. Wenn sich heute Bioinformatiker unterhalten, verstehe ich meist nicht einmal mehr, WORÜBER die überhaupt reden. Kämmerer ist weder Virologin, noch hat sie Expertise in qPCR. Und, ja, ich weiß: Verschwörungstheoretiker nörgeln allzu gerne an angeblich fehlender Expertise ihrer Gegner, mögen es aber selber gar nicht, wenn man ihnen einen krassen Mangel gerade daran nachweist.
Grüße
Andreas Beyer
Bitte anderen Texteditor verwenden. Es mussten wieder zuviele Steuerzeichen gelöscht werden.
Es darf bezweifelt werden, ob ein willkürlich festgelegter Schwellenwert oder ebenso willkürlich festgelegte Zyklen (30 Zyklen => 1.073.741.824 Multiplikationsfaktor, ~ 1 Milliarde), 40 Zyklen => 1.099.511.627.774 Multiplikationsfaktor, ~ 1 Billion) wirklich Sinn machen. ———-Aussagefähiger wäre es eher, die Anzahl der Verdopplungszyklen auszuwerten, ab denen über die Fluoreszenz-Sensorik überhaupt das detektierte und hochmultiplizierte Virus-Bruchstück erkannt werden kann. Das mag vielleicht aufwendiger sein, aber sicher näher an einem brauchbaren Ergebnis, um davon Inzidenzwerte und Lockdown-Maßnamen abzuleiten. ———-Ob unsere digitalisierungswütigen Politiker überhaupt wissen, was ein CT-Wert von 30 oder 40 bedeutet und sie 2^30 oder 2^40wirklich jemals in ihrem Leben ausgerechnet haben? Jeder Ingenieur weiß, was sich mit einem Rechnerwort mit 30 oder 40 bit darstellen läßt. Wenn in einer Ministerrunde unter Ausschalten des Parlaments dann ein stark fehlerbehafteter Inzidenzwert von 50 mal eben auf 35 heruntergesetzt wird, kann man nur eines folgern: „Denn sie wissen nicht, was sie tun“.
Langsam: so funktioniert qPCR nicht! Man lässt die Proben laufen, parallel mit einem Standard: Das ist eine log-Verdünnungsreihe mit bekannten Konzentrationen bzw. Mengen. Daran, wann diese Proben die Schwelle (threshold) überschreiten, sieht man, wie sensitiv und effizient die qPCR läuft, und zwar in Echtzeit. Ob ich die PCR dann 30 oder 3000 Zyklen laufen lasse, ist völlig unerheblich. Es ist erschreckend, dass Borger & Co das nicht begreifen, das gehört heute zum Lehrinhalt des Biochemie-Studiums.
Grüße
Andreas Beyer
Bitte anderen Texteditor verwenden. Es mussten wieder zuviele Steuerzeichen gelöscht werden.
Kommentar eines blutigen Laien. Zunächst fällt in dem Artikel auf, dass zuerst eine volle Breitseite gegen die Autoren als fachfremde Kreationisten abgefeuert wird. Nun zu den Punkten:1) Hier werden die Begriffe RNA und D(i-R)NA wahllos durcheinander geworfen. Da es sich beim SARS-Cov-2 Virus um einen RNA-Virus handelt, sind die Bildteile A und B, in denen die Aufspaltung von DNA gezeigt, wird völlig unsinig. Nach meinem Kenntnisstand docken die Primer rechts und links der Sondenstelle an und nicht an dem einem und anderen RNA-Strang der DNA. (Der zweite Strang ist bei SARS-Cov-2 gar nicht vorhanden). Desweiteren wird nur die Sonden-Stelle kopiert und nicht das Genom rechts bzw. links vom Primer. Somit sind auch die Teilbilder C und D sehr fragwürdig.Primer und Sonden können keine „DNA-Stückchen“ sein, da DNA nirgendwo andockt.Nur RNA kann an RNA oder an einem aufgespleissten DNA Strang andocken. 3) Jeder Virologe weiß auch, dass nur intakte Viren eine Infektion auslösen können. Somit ist der Test ein Indikator aber kein Nachweis einer Infektion.5), 6), 7) Über die Wichtigkeit des Ct-Werts wurde bereits genügend diskutiert. Bei genügend Zyklen kann man das Virus auch in einer Grapefruit nachweisen. Bei allen drei Punkten wird immer wieder auf Tests und Validierungen verwiesen. Leider hatten die Autoren Drosten et. al. nach eigenen Angaben keine SARS-Cov-2 Viren zur Verfügung.Der Test wurde aufgrund von SARS-Cov entwickelt.9) In einer wichtigen Tabelle wird die Einheit nM (nanoMol) mehrfach mit der Einheit nm (nanoMeter) verwechselt. (Wie lang ist ein Liter Milch?). Solche Flüchtigkeitsfehler werden normalerweise bei einer Begutachtung sofort erkannt. Das ist m.E. ein Indiz, dass der Artikel einfach durchgewunken wurde. Somit ist auch Punkt 10 dikussionswürdig.
„…SARS-Cov-2 Virus um einen RNA-Virus handelt, sind die Bildteile A und B, in denen die Aufspaltung von DNA gezeigt“
Retroviren schreiben sich selber in DNA um (Rev. Transkriptase RT); bzw. die geerntete Covid-RNA wird in vitro vor der PCR umgeschrieben (Industrie-RT). Ist ein Detail, das leicht untergeht in der Darstellung.
„da DNA nirgendwo andockt“ Doch, das ist gerade der Knackpunkt. Die Primere sind komplementär zum aufgeschmolzenen DNA-Strang und „kleben“ dort via Wasserstoffbrücke.
Danke für die Richtigstellung!
immer doch
>> dass zuerst eine volle Breitseite gegen die Autoren als fachfremde Kreationisten abgefeuert wird.<<
Wie gesagt: Skills matter, Expertise ist wichtig. Erst recht, wenn derart Haar sträubende Fehler im Text sind.
>> 1) Hier werden die Begriffe RNA und D(i-R)NA wahllos durcheinander geworfen. Da es sich beim SARS-Cov-2 Virus um einen RNA-Virus handelt, sind die Bildteile A und B, in denen die Aufspaltung von DNA gezeigt, wird völlig unsinnig. Nach meinem Kenntnisstand docken die Primer rechts und links der Sondenstelle an und nicht an dem einem und anderen RNA-Strang der DNA. (Der zweite Strang ist bei SARS-Cov-2 gar nicht vorhanden).<<
Sorry, aber da geht ALLES durcheinander. Corona hat ein RNA-Genom, richtig. Aber mit RNA kann man keine PCR machen, man schreibt sie vorher per Reverser Transkription in cDNA um, damit macht man dann PCR. Und, nein, die beiden Primer (forward und reverse) docken NICHT am selben Strang an, das wäre völliger Unsinn, sie binden gegenläufig an die beiden komplementären Stränge.
>> Desweiteren wird nur die Sonden-Stelle kopiert und nicht das Genom rechts bzw. links vom Primer. Somit sind auch die Teilbilder C und D sehr fragwürdig.<<
Bitte einfach mal genau hinschauen…
>> Primer und Sonden können keine „DNA-Stückchen“ sein, da DNA nirgendwo andockt. Nur RNA kann an RNA oder an einem aufgespleissten DNA Strang andocken.<<
Oh weh … bitte einfach mal die Begriffe „Komplementarität“ und „Hybridisierung“ recherchieren oder sich erklären lassen…
>> Jeder Virologe weiß auch, dass nur intakte Viren eine Infektion auslösen können. <<
… so wie jeder Virologe auch weiß, dass JEDWEDES Virus-Genom – intakt oder defekt, komplett oder fragmentiert – von einer Zelle produziert wurde, die mit einem intakten Virus infiziert ist.
>> Somit ist der Test ein Indikator aber kein Nachweis einer Infektion.<<
Naja … Der Test weist das SARS-CoV-2 Genom nach (ob intakt oder nicht) und somit, dass der Proband Kontakt mit (intakten) SARS-CoV-2 Viren hatte. Zumeist ist er dann auch infiziert, denn wenn ich nur Aerosol mit Viren einatme, das Virus bei mir aber nicht „Fuß fassen“ kann, ist der Titer viel zu gering für einen Nachweis. Ob ich – sofern infiziert – erkranke, steht auf einem GANZ anderen Blatt. Aber außer den Corona-Leugnern behauptet ja auch niemand, dass beides – infiziert und erkrankt – dasselbe ist.
>> Über die Wichtigkeit des Ct-Werts wurde bereits genügend diskutiert. Bei genügend Zyklen kann man das Virus auch in einer Grapefruit nachweisen. <<
Bitte einfach mal zur Kenntnis nehmen, was eine Endpunkt- und was eine RealTime-qPCR ist. Ich hab’s erklärt – s. mein Beitrag.
>> Bei allen drei Punkten wird immer wieder auf Tests und Validierungen verwiesen. Leider hatten die Autoren Drosten et. al. nach eigenen Angaben keine SARS-Cov-2 Viren zur Verfügung. <<
Auch dazu: Bitte einfach mal im Paper bzw. in der Detailanalyse nachlesen: http://ag-evolutionsbiologie.net/pdf/2021/Drosten-PCR-Borger-Report.pdf
Hallo Andreas,
es gibt keine Viren. Die Virologie ist keine Wissenschaft sondern ein Betrug. Das behauptete SARS COV-2 ist ein Computermodell.
LG
Bitte hier nur unter vollem Klarnamen posten, siehe Regeln.
Im Anschluss an den Beitrag von G.Salk kann ich nur beitragen: Wie will man einen Genabschnitt spezifisch einem Virus zuordnen, das man bis heute immer noch nicht isoliert hat. Der spanischen Fachzeitschrift „DSalud“ ist in der Novemberausgabe 2020 eine aus meiner Sicht gut begründete Kritik am Drosten PCR-Test zu entnehmen :https://www.dsalud.com/revistas/numero-242-noviembre- 202 Jesus Garcia Blanco: Abstract:Die genetischen Sequenzen, die in PCRs zum Nachweis von vermutetem SARS-CoV-2 und zur Diagnose von Krankheits- und Todesfällen verwendet werden, die auf Covid-19 zurückgeführt werden, sind in Dutzenden von Sequenzen des menschlichen Genoms selbst und in denen von etwa hundert Mikroben vorhanden. Und dazu gehören die Initiatoren oder Primer, die umfangreichsten Fragmente, die nach dem Zufallsprinzip aus ihrem vermeintlichen „Genom“ entnommen wurden, und sogar die sogenannten „Zielgene“, die angeblich spezifisch für das „neue Coronavirus“ sind. Der Test ist wertlos, und alle bisher erzielten „positiven“ Ergebnisse sollten wissenschaftlich entkräftet und den Betroffenen mitgeteilt werden; und wenn sie verstorben sind, ihren Angehörigen. Stephen Bustin, einer der weltweit führenden Experten auf dem Gebiet der PCR, sagt in der Tat, dass jeder unter bestimmten Bedingungen positiv testen kann! weiter unten :„…aber das Wichtigste ist, dass wir weiterhin Fragmente der vermeintlichen „Zielsequenz“ von SARS-CoV-2 sowohl in Mikroben als auch in unserem eigenen Genom finden. Wirklich erstaunt haben wir einen weiteren Schritt gemacht und mit dem damals als das spezifischste von SARS-CoV-2 betrachteten Gen getestet, dem E-Gen, das die Hüllproteine erzeugen soll und zwischen den Positionen 26.245 und 26.472 liegt: ATGTACTCATTCGTTTCGGAAGAGACAGGACAGGTACTACGTTAATAGTTAATAGCGTACTTCTTGCT TGCTTTCGTGGTGGTATTCTTGCTGTTACACTAGCCATCCTGCTTCGATTGTGCGCTGCTGCTGCAATA TTGTTAACGTGAGTCTTGTAAAACCTTTACGTTTACGTTTACTCGTGTGTTAAAATCTGAATCTTCTAG AGTTCGATTCTGGTCTAA. Wir wiederholten damit die bereits beschriebenen Schritte, und das Ergebnis war um so überraschender, als trotz seiner Länge weitere hundert Mikrobensequenzen mit einem Identitätsprozentsatz von 100 % und 10 Sequenzen des menschlichen Genoms mit einem Identitätsprozentsatz zwischen 80 % und 100 % auftauchten. Und ähnliche Ergebnisse wurden mit einem zufällig ausgewählten Fragment und mit dem N-Gen erzielt, das angeblich den Proteinen des Nukleokapsids SARS-CoV-2 entspricht.“ SCHLUSSFOLGERUNGENDie Konsequenz all dessen, was wir gerade erklärt haben, ist klar und unmittelbar: ES GIBT KEINEN GÜLTIGEN TEST ZUR ERKENNUNG VON SARS-COV-2,
>> [Dr. Uwe Erfurth] Wie will man einen Genabschnitt spezifisch einem Virus zuordnen, das man bis heute immer noch nicht isoliert hat.<<
Selbstverständlich ist das Virus mittlerweile isoliert, es gibt Zellkultur-Tests, es sind Virus-Genome in mittlerweile unzähligen Varianten kloniert und die Genomsequenzen in öffentlich zugänglichen Datenbanken abgelegt.
>> [Dr. Uwe Erfurth] Der spanischen Fachzeitschrift „DSalud“ ist in der Novemberausgabe 2020 eine aus meiner Sicht gut begründete Kritik am Drosten PCR-Test zu entnehmen: https://www.dsalud.com/revistas/numero-242-noviembre- 202 Jesus Garcia Blanco: Abstract: Die genetischen Sequenzen, die in PCRs zum Nachweis von vermutetem SARS-CoV-2 und zur Diagnose von Krankheits- und Todesfällen verwendet werden, die auf Covid-19 zurückgeführt werden, sind in Dutzenden von Sequenzen des menschlichen Genoms selbst und in denen von etwa hundert Mikroben vorhanden. <<
Das ist erschreckend und es zeigt, dass der Autor nicht die blasseste Ahnung hat. Bereits unsere Studierenden haben gelernt, wie man Sequenzen in der Genbank sucht (in Seq-Datenbanken nach ähnlichen Sequenzen suchen = BLASTen) und wie man diese Ähnlichkeiten analysiert und bewertet (u.a. p-value). Mit ein klein wenig Handwerkszeug kann sich JEDER selbst überzeugen, dass Corona-Sequenzen nicht im Humangenom vorkommen. Die Behauptungen sind schockierend und peinlich.
Ist das nicht auch eine Behauptung, dass CoV-2 isoliert wurde ? Wo bitte schön ? Sie haben vergessen, die Mikroben zu erwähnen, wo 100%ige Übereinstimmung gefunden wurde. Vermutlich haben Sie die spanische Arbeit gar nicht gelesen. Mögen sich die Wirrologen weiter streiten. Unbestritten ist wohl, dass ein PCR-Test keine Infektion anzeigen kann. Der PCR-Test ist aber genutzt worden, Panik zu erzeugen: 1,2 Millionen Tote in 3 Monaten hat das Strategiepapier des BMI vorhergesagt. Die CDC-USA hat zugegeben, dass eine Überprüfung der Totenscheine bestätigt hat, dass nur 6 % dem Corona-Virus zuzuordnen sind ! Das wären bei uns ca. 4.150 ! und nicht fast 70.000. Unbestreitbar fliesst Geld für gefälschte Totenscheine. In was für einem Land leben wir inzwischen? Drosten hätte von Anfang deutlich sagen müssen, dass der PCR-Test zum Nachweis von Infektionen ungeeignet ist, zumal bei einem CT-Wert von 45. Wer den Drosten-Test schön reden will, macht sich gemein mit dieser im Weimar-Urteil als kriminell bezeichneten Bande. Wie war das? Wichtig ist was hinten raus kommt !
Da ich die Sache nicht fachlich beurteilen kann, muss ich aber an das Innenministerium (Seehofer) erinnern, der gute Herr hat ein Gutachten über eine dramatische Lage der Epidemie in Auftrag gegeben. Dieses Gutachten wurde vom RKI und andere Bundeseinrichtungen geliefert wie bestellt.RKI, da war doch was ich meine Herr Drosten, hat dieser Herr nicht etwas mit dem PCR-Test zu schaffen? Den Rest kann sich jeder selbst ausmalen wie er möchte.Meine Meinung, wer solche Gutachten zu diesen Zweck (Lookdown) erstellt dem wird jedes Mittel recht sein solange er üppig bezahlt und gedeckt wird. Da spielt dann die Realität und Wahrheit keine Rolle mehr.
Was Prof. A. Beyer von der Westfälischen Hochschule hier abliefert, hat mit „wissenschaftlicher Diskussion“ absolut nichts zu tun! Das wird bereits in der Einleitung deutlich. Unter „Zunächst fällt auf…“ wie auch am Ende des Pamphlets wird wissenschaftsfeindlich ad hominem argumentiert, wobei sich Prof. A. Beyer auch nicht zu Schade ist, seine Leser klassisch hinters Licht zu führen, indem er behauptet, dass nur fachfremde Personen „bis hin hum 3D-Künstler“ Drosten kritisieren. R. Malhotra ist zwar auch künstlerisch im 3D-Bereich tätig, arbeitet aber an wissenschaftlichen Visualisierungen im Zentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften – ist also ein ausgewiesener Fachmann, so wie die anderen Autoren auch! Prof. A. Beyer kritisiert dann, dass sich nur ein Virologe unter den Autoren bei Borger et. al. befindet – er selbst ist aber auch kein Virologe! So geht es dann weiter, denn unter „Zweitens“ findet man bei Prof. A. Beyer eine klassische Argumentation gegen jede Wissenschaft, bei der auch wieder eine Art Konsens beschworen wird. Unter „Drittens“ will Prof. A. Beyer seine Leser für dumm verkaufen, denn auch seine Arbeit ist ja dann nach seinen eigenen Gesichtspunkten nicht wissenschaftlich publiziert, das Drosten-Papier hält klassischen Standards einer Veröffentlichung auch nicht stand (ohne dass ich diesen Umstand als negativ bewerte, denn der Inhalt ist entscheidend und nicht die Art des Publizierens) und dass Borger et. al. im Eurosurveillance nicht veröffentlicht werden wird, liegt wohl nicht an der Qualität sondern am Fazit oder glaubt wirklich jemand, dass Prof. Drosten in seiner eigenen Zeitschrift ein paper veröffentlicht, dass seinen PCR-Test dermaßen scharf attakiert?Diese Art der Argumentation zieht sich dann durch den gesamten Artikel. Prof. A. Beyer geht dabei offensichtlich mit schöner Selbstverständlichkeit davon aus, dass der Leser an keinem Punkt seiner Argumentation die Grundfrage der Wissenschaft „Stimmt denn das?“ stellt, denn sonst würde der Leser (egal von welchem wissenschaftlichen Niveau aus) mit Sicherheit fündig: Nein!
So ist es.
>> [Ubert Langer] Was Prof. A. Beyer von der Westfälischen Hochschule hier abliefert, hat mit „wissenschaftlicher Diskussion“ absolut nichts zu tun! Das wird bereits in der Einleitung deutlich. Unter „Zunächst fällt auf…“ wie auch am Ende des Pamphlets wird wissenschaftsfeindlich ad hominem argumentiert, wobei sich Prof. A. Beyer auch nicht zu Schade ist, seine Leser klassisch hinters Licht zu führen, indem er behauptet, dass nur fachfremde Personen „bis hin hum 3D-Künstler“ Drosten kritisieren. R. Malhotra ist zwar auch künstlerisch im 3D-Bereich tätig, arbeitet aber an wissenschaftlichen Visualisierungen im Zentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften – ist also ein ausgewiesener Fachmann, so wie die anderen Autoren auch!<<
Ich fasse es nicht. Ich meine, derart die Augen vor der Realität zu verschließen, das GEHT DOCH GAR NICHT? Nochmals, langsam und zum Mitschreiben: R. Malhotra „arbeitet an wissenschaftlichen Visualisierungen“ – ernsthaft jetzt? Hat er je mit Corona-Viren gearbeitet, sie untersucht? Je einen PCR-Test gemacht? KEINER der Autoren hat je mit Corona gearbeitet, keiner hat eigene Erfahrung mit qPCR. Faktum. Und nochmals: Der Hinweis auf fehlende Expertise und schlechte Argumentation ist kein ad hominem Argument.
>> [Ubert Langer] Prof. A. Beyer kritisiert dann, dass sich nur ein Virologe unter den Autoren bei Borger et. al. befindet – er selbst ist aber auch kein Virologe!<<
Herrlich. Umkehr der Beweislast, ein für Pseudowissenschaftler typisches Vorgehen. Wer etablierte und anerkannte Wissenschaft kritisieren will (das Corman-Drosten-Paper wurde bereits tausende Male WISSENSCHAFTLICH zitiert, der Test wird weltweit verwendet und wurde längst weiter entwickelt, u.a. von einer meiner Absolventinnen), der sollte sich der wissenschaftlichen Gemeinde stellen. Und, ja, Expertise und Fachkenntnis wäre SEHR hilfreich.
>> [Ubert Langer] Unter „Drittens“ will Prof. A. Beyer seine Leser für dumm verkaufen, denn auch seine Arbeit ist ja dann nach seinen eigenen Gesichtspunkten nicht wissenschaftlich publiziert.<<
Ich überhöre jetzt einfach mal die Unverschämtheit und antworte nur in der Sache: Bitte o.g. Logik nicht umkehren: Beweispflichtig ist nicht, wer auf einen hinreichend bestätigten Sachverhalt verweist, sondern wer ihn kritisiert. Der Kritiker muss beweisen, dass der Mond aus grünem Käse besteht, nicht ich muss jetzt selber beweisen, dass er aus Stein ist. Daher wird auch kein Fachjournal dieser Welt je ein Paper veröffentlichen mit dem Titel „Doch, Quanten existieren!“, „Doch, Raum und Zeit sind relativ!“ und „Doch, Evolution findet statt!“. Und daher wird auch logischerweise kein Fachjournal je meine Analyse publizieren.
>> [Ubert Langer] das Drosten-Papier hält klassischen Standards einer Veröffentlichung auch nicht stand<<
Eine Falschbehauptung, ein Irrtum wird durch Wiederholung nicht wahrer.
>> [Ubert Langer] dass Borger et. al. im Eurosurveillance nicht veröffentlicht werden wird, liegt wohl nicht an der Qualität sondern am Fazit oder glaubt wirklich jemand, dass Prof. Drosten in seiner eigenen Zeitschrift ein paper veröffentlicht, dass seinen PCR-Test dermaßen scharf attakiert?<<
Ganz einfach: Borger & Co sollen in einem anderen Journal publizieren … mal abwarten …
>> [Ubert Langer] Prof. A. Beyer geht dabei offensichtlich mit schöner Selbstverständlichkeit davon aus, dass der Leser an keinem Punkt seiner Argumentation die Grundfrage der Wissenschaft „Stimmt denn das?“ stellt, denn sonst würde der Leser (egal von welchem wissenschaftlichen Niveau aus) mit Sicherheit fündig: Nein!<<
Nun, ich kann (und WILL) niemanden zwingen, Fakten anzuerkennen, Ich biete sie nur denjenigen an, die WIRKLICH an Fakten interessiert sind. Details siehe http://ag-evolutionsbiologie.net/pdf/2021/Drosten-PCR-Borger-Report.pdf
Ein wissenschaftlicher Diskurs ist ja eigentlich eine gute Idee. Wir reden aber hier über Dinge, die von xxxxxxxx benutzt werden, denn offener Verfassungsbruch ist kein Kavaliersdelekt. Wissenschaftler, die xxxxxx ihrer „Expertise“ direkt oder indirekt decken oder erst ermöglichen, sollten keine Plattform bekommen, zumal diese ja auch nicht diskutieren wollen, sondern zu Gunsten ihrer Kariere alle Anderen vernichten, ins Abseits stellen, oder zumindest lächerlich machen wollen.So wie der Staat üblicherweise nicht mit Kriminellen & Terroristen verhandelt, sollten wir mit xxxxxxx Staatsvertretern oder deren Auftragswissenschaftlern ebenso verfahren. Wir können aber Material für eine spätere Abrechnung (=Anklage) zusammentragen. Das wäre eine gute Idee und beinhaltet auch mögliche Kritik an eigenen Denkfehlern. Sonst wird sich nichts ändern.
Bitte mäßigen Sie Ihre Ausdrucksweise. Wenn Sie Tatsachenbehauptungen über bestimmte Personen oder Kreise aufstellen, dann müssen Sie die beweisen. Wenn dann ein Gericht Ihrer Behauptung auch folgt, erst dann dürfen Sie sie verwenden.
Lieber Herr Limburg, ich würde gerne die vielleicht vulgäre Ausdrucksweise – die Herr Hotner eventuell gebraucht haben könnte – lesen können 🙂 Oder ist das Hatespeech? Was ist mit den Hasstaten der bösartig und genozidalen Herrscher? Mir ist neuerdings – das ist mir vollkommen fremd an mir – auch sehr nach dem Gebrauch von äußerst vulgärer Ausdrucksweise im Angesicht dieser vollkommen unfassbaren Vorgänge der überaus vulgären, verlogenen, genozidalen, perversen Herrscher im besten Deutschland, das wir je hatten 🙂
Wir sind ja ein unabhängiges Institut und haben viele Gegner mit „anderen“ Interessen. Die lassen nichts unversucht, uns schlecht zu machen. Fäkalische Ausdrucksweise, oder Extremistisches wird uns dann gern in die Schuhe geschoben. Muß nicht sein.
Hotner….
Absolut richtig….. und wissen Sie warum Libertäre und Konservative heute vielerorts in einer so misslichen Lage sind ? Ja eben, weil wir Demokratie und Meinungsfreiheit viel mehr achten wie das Sozipack. Wir versuchen Meinungsfreiheit mit potentiellen Diktatoren zu praktizieren.
Das ist etwas so klug wie einen Pädophilen zum Kindergärtner zu machen.
Bei derlei Tun gewinnen die Skrupellosen nahezu immer.
Deswegen fährt uns jede Ideologie über den Haufen.
>> [Roth Walter] Nun ja, den PCR-Test könnte man wohl verwenden, aber nicht mit 40-45 facher Verfielfältigung, sogenannten Zyklen.<<
Nochmals: So funktioniert das nicht – s.o.
Jetzt fällt der Groschen langsam. Man geht einem ungeheuerlichen Verdacht nach. Dabei war es von Anfang an so offensichtlich. „Hat China die Folgen von Corona übertrieben und harte Maßnahmen simuliert, um die Welt in zerstörerische Lockdowns zu treiben?“https://deutsche-wirtschafts-nachrichten.de/509620/Hat-China-die-Folgen-von-Corona-uebertrieben-und-harte-Massnahmen-simuliert-um-die-Welt-in-zerstoererische-Lockdowns-zu-treiben
Jonas Salk war übrigens ein berühmter Impfstofferfinder. Polio
Wir sind aber nicht verwandt. Mein Name kommt aus Griechenland. Eigentlich Schalk – S mit einem Häkchen unten wurde als S übernommen.
Nun ja, den PCR-Test könnte man wohl verwenden, aber nicht mit 40-45 facher Verfielfältigung, sogenannten Zyklen.Bei 30 Zyklen wäre das akzeptabel, denn dann würde der Test immer noch Fehler machen, aber es würden sich die Positiv-Reszultate in einem gesünderen Rahmen bewegen.Wer dann noch Positiv getestet würde, ist sehr viel wahrscheinlicher in echt Corona Positiv.Nun ist aber die Frage….. gibt es Corona so wirklich oder haben wir es nur mit einer neuen Grippe zu tun….? TODESSTOSS FÜR CORONA-PCR-TEST-REGIME? (VIDEO)Veröffentlicht am 27. Januar 2021 https://orbisnjus.com/2021/01/27/todesstoss-fuer-corona-pcr-test-regime-video/Die irische Molekularbiologin und Immunologin, Prof Dr. Dolores Cahill, die auf einen beeindruckenden Lebenslauf zurückblicken kann, hat kürzlich gegenüber James Corbett vom Corbett-Report bekanntgegeben, dass sie beabsichtige ein Projekt ins Leben zu rufen, um die Sequenzierung von PCR-Tests voranzutreiben.Weiter unter dem Link……
„Bei 30 Zyklen wäre das akzeptabel,“
Mittlerweile wird verlautbart, daß man die hinteren Ct-Signale als nicht mehr vertrauenswürdig einstuft. Der Test gilt dann als negativ.
@Herrn Krüger: Sehr schön dargestellt was nach dem „Wichtig für den ärztlichen Befund ist:“ folgt!!!Aber unser Land wird von psychopath-kriminellen Politikern rein aufgrund des PCR-Tests an die Wand gefahren. Da kommt kein ärztlicher Befund und ein Zweittest nur bei Sport-Promis, die nach dem ersten Positiv-Test wohl gesagt bekommen, welches Labor sich für negative Ergebnisse eignet.
@Herr Friedrichs: nicht zu vergessen, dass es ein Patent auf das „neuartige Coronavirus“ gibt. Alle patentierten Krankheiten sind im Labor erschaffen. Christian Anders hat ein Buch namens „The man, w.h.o. created aids“ und eines namens „Der Impfwahnsinn“ geschrieben, die sind sehr erhellend.
Fachlich kann ich das zwar nicht beurteilen. Die Beurteilung von Beyer kommt mir jedenfalls vor wie bestellte Blendgranaten. In solchen Fällen hilft Helmut Kohl weiter, der sagte: entscheidend ist was hinten heraus kommt. Und da kam es doch haufenweise zu falschen Testergebnissen. Warum auch immer. Zu Recht wird hier an Tönnies erinnert. Die Praxis hat Beyer also schon längst widerlegt.
>> (Raimund Könighaus, Sabine Interthal] nicht zu vergessen, dass es ein Patent auf das „neuartige Coronavirus“ gibt<<
Ganz grobes Missverständnis. Viren und Bakterien kann man nicht patentieren. Man kann nur künstlich Geschaffenes patentieren, also z.B. ein rekombinantes oder attenuiertes Impfvirus. Nicht aber natürlich vorkommende Entitäten, und damit auch nicht SARS-CoV-2. Darauf gibt es kein patent und wird es auch nie geben.
>> [Raimund Könighaus] Fachlich kann ich das zwar nicht beurteilen. Die Beurteilung von Beyer kommt mir jedenfalls vor wie bestellte Blendgranaten. In solchen Fällen hilft Helmut Kohl weiter, der sagte: entscheidend ist was hinten heraus kommt. Und da kam es doch haufenweise zu falschen Testergebnissen. Warum auch immer. Zu Recht wird hier an Tönnies erinnert. Die Praxis hat Beyer also schon längst widerlegt.<<
Interessant. Warum wurde und wird der Drosten-Test denn weltweit angewendet? Tausende von Malen wissenschaftlich zitiert? Warum ist er – jetzt mit der Verfügbarkeit umfassender Sequenzinformation – längst Ausgangspunkt für die Entwicklung einer zweiten und dritten Generation von SARS-CoV-2-qPCRs? Längst widerlegt, aha …
Soweit ich das hier verfolge, wurde jetzt hier eine fundiert wirkende Kritik abgedruckt, die eine frühere Kritik kritisiert. Das steht einer Diskussion mit Niveau gut zu Gesicht – auch wenn es einem unbeliebten Herrn Drosten hilft. Notfalls muss man sein Weltbild halt auch mal korrigieren, wenn es überzeugende Gegenargumente gibt. Das gilt sogar für das „Weltklima“ – ich warte noch…
Meine Güte, was für ein Unsinn. Dass Drosten ein Scharlatan ist, dass ist doch hinlänglich bewiesen. Da muss ich auch kein „Wirrologe“ für sein, da reicht der gesunde Menschenverstand. Der Komiker Drosten widerspricht sich doch fortlaufend, wechselt seine Meinung so wie andere die Unterhose…
>>[Ruud Jarstein] dass Drosten ein Scharlatan ist, dass ist doch hinlänglich bewiesen. Da muss ich auch kein „Wirrologe“ für sein, da reicht der gesunde Menschenverstand.<<
https://de.wikipedia.org/wiki/Dunning-Kruger-Effekt
https://en.wikipedia.org/wiki/The_Death_of_Expertise
Meiner Info nach laufen die aktuellen PCR-Tests so ab.Viele Labors in Deutschland testen dabei nicht nur auf einen, sondern auf mindestens zwei Genabschnitte („Dual-Target“-System). Das reduziert die Wahrscheinlichkeit für sogenannte falsch-positive Ergebnisse zusätzlich.Zur Sicherheit weisen die PCR-Tests meistens zwei oder drei verschiedene Bereiche im Erbgut des Virus nach.Wichtig für den ärztlichen Befund ist: Nur wenn die in jedem Testlauf mitgeführten Positiv- und Negativkontrollen korrekt verlaufen und es keine untypischen Kurvenverläufe gibt, wird der Test zu einer Befundung herangezogen“, erläutert die Fachgesellschaft.Nur nach dieser technischen Validierung gehe das Ergebnis an den Laborarzt. Sei das Ergebnis zweifelhaft, weil zum Beispiel nur ein Genabschnitt von zwei oder drei im Testsystem nachzuweisenden erfolgreich vervielfältigt wurde, dann werde der Test mit einem PCR-Test eines anderen Herstellers wiederholt oder es werde eine neue Probe des Patienten angefordert.„Erst wenn das Testergebnis technisch einwandfrei ist, wird es für den Befund herangezogen“, so die Fachgesellschaft.
Nun ja, Krüger……
Tatsache bleibt, das Gensequenzen noch keinen Virus nachweisen.
Der wissenschaftkliche Nachweis wäre gegeben wenn man die Gensequenzen zur Gänze aufgeschlüsselt hätte, das sind dann ca. 40ooo Paare und oder wenn man eine Probe so gereinigt hat das man das Virzus separrieren, visualisieren konnte.
Das ist bei Corona nicht gegeben.
Wir testen etwas mit 1 oder 1 Gensequenzen ……… was aber auch einfach eine Influenza neuen Typs sein könnte.
Wissenschaftlich ist Corone vbislang nicht nachgewiesen.
Nein, was wir nun ist quasi zu sagen ist …… das wenn das Essen scharf ist, muss auch Pfeffer drinn sein. Nein so geht das nicht.
>> [Roth Walter] Tatsache bleibt, das Gensequenzen noch keinen Virus nachweisen. Der wissenschaftkliche Nachweis wäre gegeben wenn man die Gensequenzen zur Gänze aufgeschlüsselt hätte, das sind dann ca. 40ooo Paare und oder wenn man eine Probe so gereinigt hat das man das Virzus separrieren, visualisieren konnte.<<
Missverständnis, s.o.: Jedes Corona-Genom, ob intakt oder defekt, ob komplett oder fragmentiert, stammt von einer Zelle, die von einem intakten Corona-Virion erfolgreich infiziert wurde.
Ja, wäre es aber nicht sinnvoll die PCR gegen einen Plaguetest zu validieren? Was sagt uns eine PCR Probe mit einem Ct=14 die bei einem symptomfreien „Patienten“ gefunden wurde? Ich kann Argument 3 nicht nachvollziehen.
Fragt sich nur noch nach welchen Genabschnitten getestet wird. Einer Kuh, eines Mehrschweinchens, eines Aliens oder einer Schlange.
Der war gut 🙂
>> [Guntbert Salk] Fragt sich nur noch nach welchen Genabschnitten getestet wird. Einer Kuh, eines Mehrschweinchens, eines Aliens oder einer Schlange.<<
Guter Witz – einfach mal ins Corman-Drosten-Paper schauen, da steht’s explizit und in aller Breite drin. Und wer’s nicht glaubt, kann die Primer- und Sondensequenzen selber im NCBI (GenBank) oder der Japan- oder der EMBL-Gendatenbank DDBJ bzw. EMBL-Bank) BLASTen und sich selber überzeugen.
„Erst wenn das Testergebnis technisch einwandfrei ist, wird es für den Befund herangezogen“.
So soll es sein. Müßte eigentlich nicht mehr erwähnt werden; aber gut, in Muttis Deutschland wird es nötig. Es bleibt aber dabei: Wenn zwei oder drei Sequenzen nachgewiesen wurden, heißt das Corona. Welches, ist fraglich, Schnupfen ist neben Rhinoviren meist auf Corona zurückzuführen. Zoonose übrigens, Tönnies zeigt es.
Und selbst wenn die PKR nur auf Sars2 und seine Mutanten anspränge: Sie müssen nicht infiziert sein, oder nicht mehr, oder noch nicht… Infektion heißt: Virus ist in nennenswerter Zahl im Zielgewebe, IN den Zellen. Alles andere ist zu schwammig für irgendeine Aussage wie „Inzidenz“
>> [Axel Robert Göhring] Zoonose übrigens, Tönnies zeigt es.<<
Nein. „Zoonose“ ist ein anderes Thema: Wenngleich der erste Sprung auf Menschen zoonotisch war, geschieht die Übertragung seit einem Jahr faktisch ausschließlich Mensch => Mensch. Und Tönnies hat mit Zoonose nun rein gar nichts zu tun: Die Schweine sind und waren nicht infiziert.
Es gibt nun wohl schon etliche Erwiderung auf meine Analyse. Gut so. Irgendwann werde ich mir die Zeit nehmen, dies alles dann zusammenzufassen, aber im Moment liegen hier 80 Klausuren, dann kommen mehrere Praktikums-Tage, nicht zu vergessen meine Forschungsprojekte, durchgeführt von meinen beiden Absolventen in meinem Lab, die ich selber betreuen muss. Im März nochmals 100 Klausuren, dazwischen Abschlussprüfungen und Gutachten. Video-Konferenzen, zu schreibende Anträge, Hochschulverwaltung, die anstehende Reakkreditierung. Pseudowissenschaft ist nur ein Hobby, und das muss nun warten: Auch diese Stunde hier ist nur gestohlen – ich gehe jetzt wieder ins Labor und schaue mir die PCR-Ergebnisse meiner Absolventin an.
Grüße
Andreas Beyer
>> [Axel Robert Göhring] Es bleibt aber dabei: Wenn zwei oder drei Sequenzen nachgewiesen wurden, heißt das Corona. Welches, ist fraglich, Schnupfen ist neben Rhinoviren meist auf Corona zurückzuführen.<<
Nein, es ist NICHT fraglich: Es wurden Sequenzbereiche gewählt, die für BETA-Coronaviren spezifisch sind, und von denen zirkuliert im Moment nur SARS-CoV-2 in der Menschheit. Und im Paper steht explizit und für jeden Fachmenschen nachvollziehbar, wie die Differenzierung gegen andere Viren vorgenommen wurde. Übrigens: Andere Viren – insbesondere alle relevanten, die im Atmungstrakt vorkommen – wurden von Corman-Drosten getestet.
Nach einer Arbeit von Jesus Garcia Blanca aus Spanien kommen die angesteuerten Gensequenzen auch im Menschen selbst und in ca. 100 Mikroben (100 x 100%ige Übereinstimmung) vor. Dies hat er durch einfachen Abgleich der publizierten Drosten-Sequenzen mit Datenbanken hearusgefunden. Da kann man wohl kaum von einer Corona-Spezifität sprechen.