Der Run auf die Energieerzeugung aus der Atomkernfusion
Aufmacherbild: Es sind drei Protonen und vier Neutronen erkennbar und drei Elektronen. Damit ist das hier das Element Lithium 7Li. (Ob hinten ein viertes Proton nicht sichtbar ist, sei dahingestellt).
Andreas Demmig
Viele Regierungen setzen nun auf intensivere Förderung der Entwicklungen zur Fusionstechnik. Man erhofft sich eine sehr große Energiequelle, ohne störende Rest-Abfälle => Atommüll.
Mit meiner Zusammenstellung möchte ich in möglichst einfacher Weise, unseren Lesern ohne ausgeprägte Physik-Kenntnisse, den Einstieg erleichtern. Mir ist bewusst, dass die heutigen Erkenntnisse, vor allem in der Quantenphysik bislang ungeahnte und sehr verwirrende Verhaltensweisen und Eigenschaften unserer Welt im kleinsten, auf denen doch alles aufbaut, eröffnet. Auch wenn das Bohrsche Atommodell inzwischen überholt ist, als Anschauung und Einstieg ist es jedoch noch immer hilfreich.
Wenn ich Ihr Interesse geweckt habe, nehmen Sie diesen Beitrag daher bitte als Anstoß, selbst weiter zu suchen.
Atom – Elemente
Die Welt besteht aus Atomen. Ein Atom besitzt einen Kern, der aus mindestens einem positiven geladenen Teilchen besteht, dem Positron und ein dazugehöriges negativ geladenes Elektron, das den Kern auf einer festgelegten Bahn umkreist. Damit ist das Atom elektrisch neutral (nach Außen). https://de.wikipedia.org/wiki/Atom
Im Kern kann / bzw. muss es noch Neutronen geben, das sind Teilchen wie die Positronen, sie haben jedoch ein Elektron „dabei“, damit sind sie im Kern elektrisch neutral. Diese Neutronen stabilisieren den Atomkern. Je mehr Protonen es gibt, um so mehr Neutronen müssen im Kern vorhanden sein, damit das Atom stabil bleiben kann, manchmal sind sogar mehr Neutronen notwendig, als Protonen vorhanden sind, damit der Kern stabil bleibt.
Elemente:
Um was für ein Element es sich handelt, ist durch die Anzahl der Positronen im Kern gekennzeichnet
- Ein Element mit einem Positron (Kern) ist der Wasserstoff, mit ca. 75% das häufigste Element im Universum, das Formelzeichen ist H (hier genutzt, um nicht immer so lange Wörter schreiben und lesen zu müssen)
- Ein Element mit zwei Positronen ist Helium, Formelzeichen He
Die Bausteine des Kerns, Protonen und Neutronen werden als Nukleonen bezeichnet.
Nun wissen Sie, dass es Atome mit mehreren Protonen gibt. Da überrascht es Sie nicht mehr, dass zum Zusammenhalten der ganzen Protonen im Kern – gleichnamige Ladung stößt sich ab, auch noch weitere neutralisierende Teilchen dabei sein müssen – Neutronen, fachlich korrekt als elektrisch neutrales Baryon oder als Nukleon bezeichnet, damit das nicht sofort auseinanderstrebt.
Fusion:
Werden zwei Wasserstoffatom-Kerne zusammengebracht -so dicht, dass sie Fusionieren, ergibt sich ein Heliumatom. Dafür wird weniger Bindungsenergie benötigt als für ein H-Atom plus noch ein H-Atom. Diese „überflüssige Bindungsenergie wird abgegeben – das ist die Energie, die unsere Sonne in Mengen abgibt.
In der nachfolgenden Grafik unten, erkennen Sie, dass zwischen ³He und 4He ein größerer Sprung in der Bindungsenergie vorhanden ist. Fusionieren / verschmelzen wir diese zu Helium, bleibt besonders viel Bindungsenergie übrig. Daher konzentrieren sich die Forscher besonders auf die Fusion dieser Isotope.
Hier die Beschreibung des US-Energieministeriums
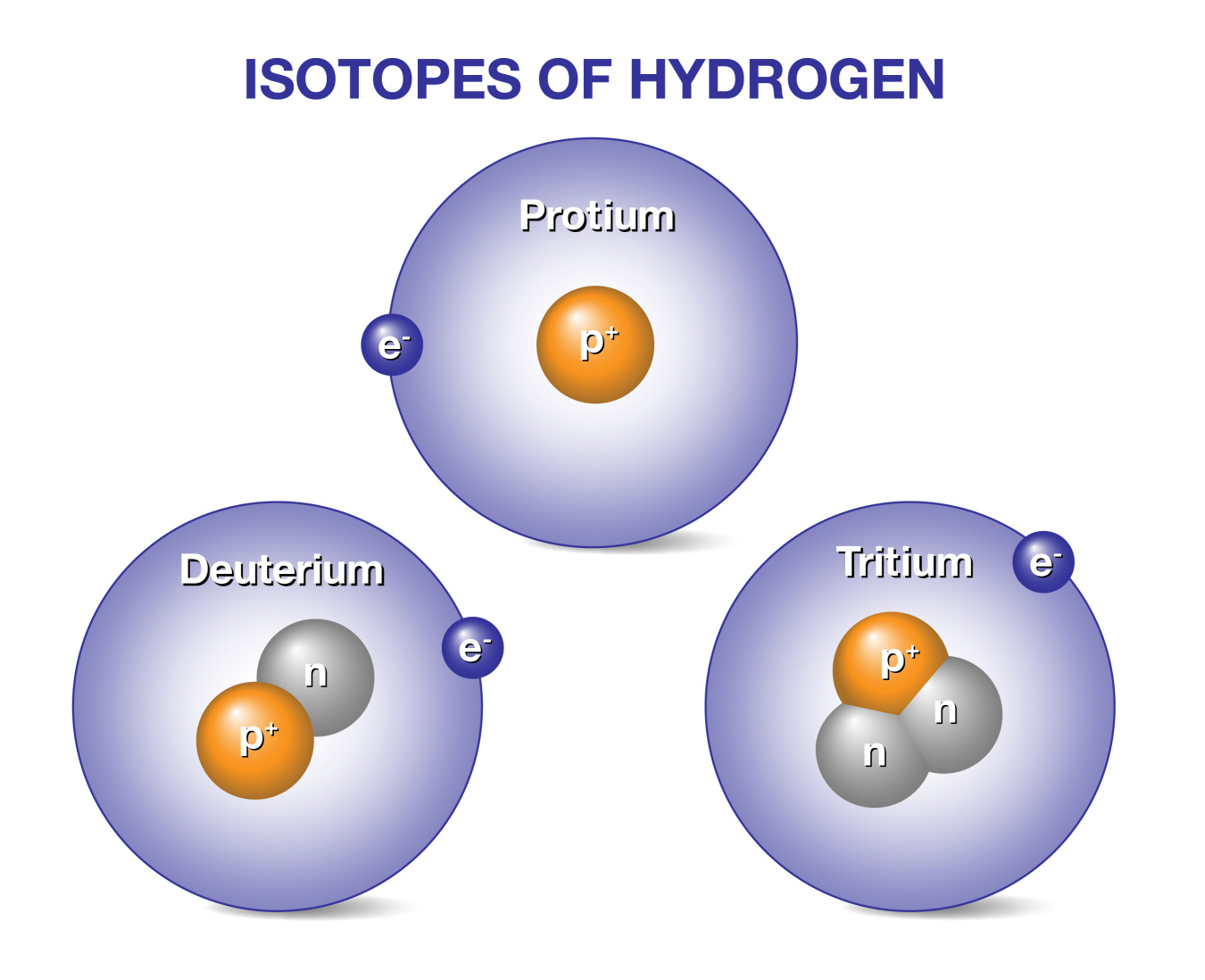
Image courtesy of General Atomics
Alle Wasserstoffisotope enthalten nur ein Proton im Atomkern, die Anzahl der Neutronen variiert jedoch. – Sind es mehr Protonen, wäre es nicht mehr Wasserstoff
Wasserstoffatome gibt es in vier bekannten Varianten – Nukleonen, nur ein Proton 1H, mit einem Neutron 2H Deuterium, mit zwei Neutronen 3H Tritium. Grundsätzlich gibt es auch ein Wasserstoffatom mit drei Neutronen, einfach Wasserstoff-4 (Symbol: 4H).
Deuterium und Tritium sind vielversprechende Brennstoffe für die Energieerzeugung in zukünftigen Fusionskraftwerken. Fusionsenergie treibt die Sonne und andere Sterne durch Kernfusion an. Deuterium und Tritium sind Isotope des Wasserstoffs, dem häufigsten Element im Universum. Während alle Wasserstoffisotope ein Proton besitzen , hat Deuterium zusätzlich ein Neutron und Tritium zwei. Daher ist ihre Ionenmasse höher als die von Protium, dem neutronenlosen Wasserstoffisotop. Bei der Fusion von Deuterium und Tritium entsteht ein Heliumatom mit zwei Protonen, zwei Neutronen und einem energiereichen Neutron. Diese energiereichen Neutronen könnten die Grundlage für die Energieerzeugung in zukünftigen Fusionskraftwerken bilden.
… Die meisten Elemente fusionieren jedoch nur im Inneren eines Sterns. Um in experimentellen Fusionskraftwerken wie Tokamaks und Stellaratoren brennende Plasmen zu erzeugen, suchen Wissenschaftler nach einem Brennstoff, der verfügbar und relativ einfach herzustellen und zu lagern ist. Eine vielversprechende Option ist Deuterium-Tritium-Brennstoff. Dieser Brennstoff erreicht die Fusionsbedingungen bei niedrigeren Temperaturen als andere Elemente und setzt mehr Energie frei als andere Fusionsreaktionen. …
Deuterium ist weit verbreitet: Etwa eines von 6.500 Wasserstoffatomen im Meerwasser liegt als Deuterium vor. Das bedeutet, dass unsere Ozeane viele Tonnen dieses Wasserstoffisotops enthalten. Die Fusionsenergie, die bei nur einem Gramm Deuterium-Tritium-Brennstoff freigesetzt wird, entspricht der Energie von etwa 2.400 Gallonen Öl.
Tritium ist selten. Es ist ein radioaktives Isotop, das mit einer Halbwertszeit von 12 Jahren relativ schnell zerfällt. In der Natur kommt es nur selten vor und steht für den Einsatz in potenziellen Kernkraftwerken nicht unmittelbar zur Verfügung. Es gibt jedoch ein Verfahren zur Tritiumerzeugung. Beispielsweise kann Tritium durch Kernspaltung mit niedriger Energie erzeugt werden, indem das häufigere Element Lithium energiereichen Neutronen ausgesetzt wird. Wissenschaftler forschen intensiv an der Tritiumerzeugung – einem Prozess namens Tritiumbrut – als Teil eines Subsystems von Fusionskraftwerken. Ziel ist es, die benötigte Menge zu produzieren, um zukünftige Kernkraftwerke tritiumunabhängig zu machen. Tritiumbrutsysteme benötigen angereichertes Lithium, insbesondere das Isotop Lithium-6 (mit drei Protonen und drei Neutronen). Da Lithium-6 deutlich seltener ist als andere Lithiumisotope, forschen Wissenschaftler intensiv an der Lithiumisotopentrennung mit Schwerpunkt auf skalierbaren und umweltfreundlichen Methoden.
https://www.energy.gov/science/doe-explainsdeuterium-tritium-fusion-fuel
Ein Beitrag einer deutschen Webseite
Das Problem des Tritiums – Gibt es genug Brennstoff für Fusionsreaktoren?
-
- Juli 2021
Schon seit Jahrzehnten wird die Kernfusion vollmundig als Energie der Zukunft beworben, als Lösung aller Energie- und Klimaprobleme. Doch der Weg dorthin ist aufwendig und zäh – und das Ganze ist nicht unumstritten – im Gegenteil. Auch in der Wissenschaft gibt es einige Stimmen, die die Stromerzeugung durch Fusionsreaktoren wie die geplanten ITER-Nachfolger für einen teuren Irrweg halten. Einer der Gründe: Obwohl die Kernfusion schon seit Jahrzehnten erforscht wird, sind einige Probleme auch bei ITER nicht vollends gelöst.
https://www.scinexx.de/dossierartikel/das-problem-des-tritiums/
Folgende Grafik ist wesentlich zum Verständnis
https://de.wikipedia.org/wiki/Datei:Atomkernbindungsenergien_pro_Nukleon_Hippler_2016.png
Die kleine Grafik vergrößert den Anfangsbereich. Die Abstände zwischen den Nukleonen (Kernbausteinen) zeigt die bei einer Fusion „nicht benötigte, abgebbare“ Bindungsenergie. Diese abgegebene Strahlung wird als Wärme abgegeben.
Weiteres zur Bindungsenergie finden Sie hier: https://de.wikipedia.org/wiki/Bindungsenergie
Mögliche Fusionsenergie
Nun wissen Sie im Groben, wie Kernfusion funktionieren soll. Es müssen genügend Wasserstoffatome als „Brennstoff“ vorhanden sein, vorzugsweise als Wasserstoff-2, Deuterium, da hier mehr Bindungsenergie übrigbleibt. Davon gibt es auf der Erde aber nur wenig, bis sehr wenig und kann / muss unter hohem Energieeinsatz hergestellt werden.
Dann müssen diese Wasserstoffelemente sehr dicht „zusammengepresst“ werden, damit sich die Kerne berühren und fusionieren. Das wird sehr heiß, in diesem Fall ist Wärme und Hitze die Bezeichnung für Energie. Der Brennstoff muss gleichmäßig weiter zugeführt werden, damit der Prozess erhalten bleibt.
In unserer Sonne
gibt es unzählige Heliumkerne, welche durch die eigene Gravitation zusammengehalten, gar zusammengepresst werden. Da gibt es das Problem der Abschirmung nicht und der Brennstoff ist gleichmäßig drumherum vorhanden.
Aber: Der Wasserstoff in der Sonne wird nicht sofort auf einmal fusioniert, weil die Kernfusion ein äußerst langsamer Prozess ist, der von extrem niedrigen Wahrscheinlichkeiten und physikalischen Barrieren abhängt, trotz der hohen Temperaturen und Drücke im Kern. Die Sonne ist keine Bombe, sondern ein stabiler Reaktor.
Pro Sekunde fusionieren in ihrem Inneren rund 600 Millionen Tonnen Wasserstoff zu 596 Millionen Tonnen Helium. Das geht schon seit rund 4,6 Milliarden Jahren so. Dieser Massenunterschied von 4 Millionen Tonnen pro Sekunde sorgt dafür, dass unsere Sonne scheint, denn er wird als Energie freigesetzt. Die Kernfusion ist der Grund, warum alle Sterne scheinen. Somit ist die Kernfusion die ultimative Energiequelle in unserem Sonnensystem, die das Leben auf der Erde überhaupt erst ermöglicht. Keine Sorge: Obwohl die Sonne jeden Moment an Masse verliert, ist noch genügend „Brennstoff“ für ein paar Milliarden Jahre übrig.
Kernspaltung – zur Abrundung
Fusionsenergie („abgebbare“ Bindungsenergie) gibt es bis zum Element Eisen, wenn auch mit abnehmbarer Energie. Elemente oberhalb von Eisen werden / wurden nur durch sehr starke Energieausbrüche, in der Natur durch explodierende Supernova gebildet (zusammengebacken). Uran-236 ist in der Grafik eingezeichnet. Diese und noch schwerere Kerne halten nicht mehr so gut zusammen, sie sind instabil und spalten sich – Kernspaltung. Diese Spaltung oder auch Zerfall genannt, passiert je nach Element über kurz oder lang. Je kürzer die Halbwertszeit, umso aktiver – radioaktiver ist das Element und umgekehrt! Je nach Anzahl der „zusammenbleibenden Nukleonen“ bleiben nach einer Kernspaltung zwei unterschiedliche Atome -> Elemente übrig. Das spalten geht nun solange, bis ein stabiler Kern übriggeblieben ist (Das passiert in unseren Kernrektoren).
Die Halbwertszeit ist die Zeitspanne, in der sich die Menge radioaktiver Atomkerne (Isotope) durch Zerfall halbiert. Diese Zeit variiert stark, von Sekundenbruchteilen bis zu Milliarden Jahren, und bleibt für ein spezifisches Isotop stets konstant. Sie ermöglicht die Altersbestimmung (z.B. C-14) und beschreibt die Strahlungsdauer.
Beispiele für Halbwertszeiten von Elementen/Isotopen:
- Uran-238: 4,468 Milliarden Jahre
- Thorium-232: 14,05 Milliarden Jahre
- Plutonium-239: 24.110 Jahre
- Cäsium-137: 30 Jahre
- Iod-131: 8 Tage
Nebenhinweis: Daraus leitet sich ab, unsere Erde und unser Sonnensystem ist die dritte Generation der Sternentstehung.
Die erste Generation schuf durch Fusionieren Elemente aus Wasserstoff bis zum Eisen, Dann verging die erste Sonne am Ende ihrer Lebensdauer in einer Supernova, dabei wurden schwere Elemente als Eisen – bis Plutonium gebildet.
Dann begann der Zyklus von neuem, Es gibt immer noch genügend Wasserstoff für die Bildung einer Sonne. Auf unserer Erde finden wir Elemente bis zum Plutonium, in unterschiedlicher Menge, das heißt, es gab bereits zwei Sonnen vor uns.
Das Periodensystem der Elemente (PSE)
ist eine Tabelle mit 118 chemischen Elementen, geordnet nach steigender Ordnungszahl (Anzahl der Protonen), die ihre chemischen Eigenschaften widerspiegelt und sie in Perioden (Zeilen) und Gruppen (Spalten) einteilt, um ähnliche Merkmale wie Valenzelektronen und Elektronenschalen zu zeigen, was Vorhersagen über ihr Verhalten ermöglicht, wie z. B. Wasserstoff (H) auf Platz 1, Sauerstoff (O) auf Platz 8, Eisen (Fe) mit dem Symbol Fe und dem lateinischen Namen ferrum https://de.wikipedia.org/wiki/Periodensystem

Von Antonsusi – Eigenes Werk, Gemeinfrei, https://commons.wikimedia.org/w/index.php?curid=82871392
Aufbau und Organisation
- Ordnungszahl (OZ): Bestimmt die Position, gibt Protonenanzahl an; steigt von links nach rechts.
- Perioden (Zeilen): Zeigen die Anzahl der Elektronenschalen an (z. B. Periode 3 hat 3 Schalen).
- Gruppen (Spalten): Elemente in derselben Hauptgruppe haben ähnliche Valenzelektronen (äußere Elektronen), was zu ähnlichen chemischen Eigenschaften führt (z. B. Hauptgruppe II: Magnesium, Calcium).
Beispiele für Elemente
- Wasserstoff (H): OZ 1, erstes Element.
- Helium (He): OZ 2, Edelgas.
- Kohlenstoff (C): OZ 6, wichtig für das Leben.
- Sauerstoff (O): OZ 8, wichtig für Leben.
- Eisen (Fe): OZ 26, Symbol von ferrum.
- Gold (Au): OZ 79, Symbol von aurum.
Entdeckung und Vorkommen
- Insgesamt 118 Elemente bekannt.
- Elemente 1–94 kommen natürlich vor (mit wenigen Ausnahmen).
- Elemente 95–118 wurden künstlich erzeugt.
Literaturhinweis:
Ich habe das nachfolgende Buch und kann es privat sehr empfehlen (m.e. Grundlagensemester der Astrophysik)
Das Dunkle Universum: Der Wettstreit Dunkler Materie und Dunkler Energie: Ist das Universum zum Sterben geboren? Gebundene Ausgabe – 12. Mai 2017
von Adalbert W. A. Pauldrach (Autor)
https://www.amazon.de/Das-Dunkle-Universum-Wettstreit-Dunkler/dp/3662529157